ರಸಾಯನಶಾಸ್ತ್ರದಲ್ಲಿ ಎಲೆಕ್ಟ್ರೋಲೈಟ್ ಎಂದರೇನು. ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳನ್ನು ಸೂಚಿಸುತ್ತದೆ. ಯಾವ ಕಣಗಳು ಚಾರ್ಜ್ ಅನ್ನು ಒಯ್ಯುತ್ತವೆ?
ಇವುಗಳು ದ್ರಾವಣಗಳು ಅಥವಾ ಕರಗುವಿಕೆಗಳು ವಿದ್ಯುತ್ ಪ್ರವಾಹವನ್ನು ನಡೆಸುವ ವಸ್ತುಗಳು. ಅವು ದ್ರವಗಳು ಮತ್ತು ಜೀವಿಗಳ ದಟ್ಟವಾದ ಅಂಗಾಂಶಗಳ ಅನಿವಾರ್ಯ ಅಂಶವಾಗಿದೆ.
ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳಲ್ಲಿ ಆಮ್ಲಗಳು, ಬೇಸ್ಗಳು ಮತ್ತು ಲವಣಗಳು ಸೇರಿವೆ. ಕರಗಿದ ಅಥವಾ ಕರಗಿದ ಸ್ಥಿತಿಯಲ್ಲಿ ವಿದ್ಯುತ್ ಪ್ರವಾಹವನ್ನು ನಡೆಸದ ವಸ್ತುಗಳನ್ನು ನಾನ್ಎಲೆಕ್ಟ್ರೋಲೈಟ್ಸ್ ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ. ಇವುಗಳು ಸಕ್ಕರೆಗಳು, ಆಲ್ಕೋಹಾಲ್ಗಳು, ಇತ್ಯಾದಿಗಳಂತಹ ಅನೇಕ ಸಾವಯವ ಪದಾರ್ಥಗಳನ್ನು ಒಳಗೊಂಡಿವೆ. ವಿದ್ಯುತ್ ಪ್ರವಾಹವನ್ನು ನಡೆಸಲು ಎಲೆಕ್ಟ್ರೋಲೈಟ್ ದ್ರಾವಣಗಳ ಸಾಮರ್ಥ್ಯವನ್ನು ಕರಗಿಸಿದಾಗ, ಎಲೆಕ್ಟ್ರೋಲೈಟ್ ಅಣುಗಳು ವಿದ್ಯುತ್ ಧನಾತ್ಮಕವಾಗಿ ಮತ್ತು ಋಣಾತ್ಮಕವಾಗಿ ಚಾರ್ಜ್ ಮಾಡಲಾದ ಕಣಗಳಾಗಿ ವಿಭಜನೆಯಾಗುತ್ತವೆ - ಅಯಾನುಗಳು. ಅಯಾನಿನ ಮೇಲಿನ ಚಾರ್ಜ್ ಪ್ರಮಾಣವು ಅಯಾನು ರೂಪಿಸುವ ಪರಮಾಣು ಅಥವಾ ಪರಮಾಣುಗಳ ಗುಂಪಿನ ವೇಲೆನ್ಸಿಗೆ ಸಂಖ್ಯಾತ್ಮಕವಾಗಿ ಸಮಾನವಾಗಿರುತ್ತದೆ. ಅಯಾನುಗಳು ಪರಮಾಣುಗಳು ಮತ್ತು ಅಣುಗಳಿಂದ ವಿದ್ಯುತ್ ಶುಲ್ಕಗಳ ಉಪಸ್ಥಿತಿಯಲ್ಲಿ ಮಾತ್ರವಲ್ಲದೆ ಇತರ ಗುಣಲಕ್ಷಣಗಳಲ್ಲಿಯೂ ಭಿನ್ನವಾಗಿರುತ್ತವೆ, ಉದಾಹರಣೆಗೆ, ಕ್ಲೋರಿನ್ ಅಯಾನುಗಳು ಯಾವುದೇ ವಾಸನೆ, ಬಣ್ಣ ಅಥವಾ ಕ್ಲೋರಿನ್ ಅಣುಗಳ ಇತರ ಗುಣಲಕ್ಷಣಗಳನ್ನು ಹೊಂದಿರುವುದಿಲ್ಲ.
ಧನಾತ್ಮಕ ಚಾರ್ಜ್ಡ್ ಅಯಾನುಗಳನ್ನು ಕ್ಯಾಟಯಾನ್ಸ್ ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ, ಋಣಾತ್ಮಕ ಚಾರ್ಜ್ಡ್ ಅಯಾನುಗಳನ್ನು ಅಯಾನುಗಳು ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ. ಕ್ಯಾಟಯಾನುಗಳು ಹೈಡ್ರೋಜನ್ ಪರಮಾಣುಗಳನ್ನು ರೂಪಿಸುತ್ತವೆ H +, ಲೋಹಗಳು: K +, Na +, Ca 2+, Fe 3+ ಮತ್ತು ಪರಮಾಣುಗಳ ಕೆಲವು ಗುಂಪುಗಳು, ಉದಾಹರಣೆಗೆ ಅಮೋನಿಯಮ್ ಗುಂಪು NH + 4; ಅಯಾನುಗಳು ಆಮ್ಲೀಯ ಉಳಿಕೆಗಳಾದ ಪರಮಾಣುಗಳು ಮತ್ತು ಪರಮಾಣುಗಳ ಗುಂಪುಗಳನ್ನು ರೂಪಿಸುತ್ತವೆ, ಉದಾಹರಣೆಗೆ Cl -, NO - 3, SO 2- 4, CO 2- 3.
E. ಎಂಬ ಪದವನ್ನು ಫ್ಯಾರಡೆ ವಿಜ್ಞಾನಕ್ಕೆ ಪರಿಚಯಿಸಿದರು. ತೀರಾ ಇತ್ತೀಚಿನವರೆಗೂ, K.E. ವಿಶಿಷ್ಟವಾದ ಲವಣಗಳು, ಆಮ್ಲಗಳು ಮತ್ತು ಕ್ಷಾರಗಳು, ಹಾಗೆಯೇ ನೀರನ್ನು ಒಳಗೊಂಡಿತ್ತು. ಜಲೀಯವಲ್ಲದ ದ್ರಾವಣಗಳ ಅಧ್ಯಯನಗಳು, ಹಾಗೆಯೇ ಅತಿ ಹೆಚ್ಚಿನ ತಾಪಮಾನದಲ್ಲಿನ ಅಧ್ಯಯನಗಳು ಈ ಕ್ಷೇತ್ರವನ್ನು ಬಹಳವಾಗಿ ವಿಸ್ತರಿಸಿವೆ. I.A. Kablukov, Kadi, Karara, P.I. ವಾಲ್ಡೆನ್ ಮತ್ತು ಇತರರು ಜಲೀಯ ಮತ್ತು ಆಲ್ಕೋಹಾಲ್ ದ್ರಾವಣಗಳು ಪ್ರವಾಹವನ್ನು ಗಮನಾರ್ಹವಾಗಿ ನಡೆಸುತ್ತವೆ ಎಂದು ತೋರಿಸಿದರು, ಆದರೆ ದ್ರವ ಅಮೋನಿಯಾ, ದ್ರವ ಸಲ್ಫರ್ ಡೈಆಕ್ಸೈಡ್ ಅನ್ಹೈಡ್ರೈಡ್ ಮುಂತಾದ ಹಲವಾರು ಇತರ ಪದಾರ್ಥಗಳಲ್ಲಿನ ಪರಿಹಾರಗಳು. ಅನೇಕ ವಸ್ತುಗಳು ಮತ್ತು ಮಿಶ್ರಣಗಳು ಸಾಮಾನ್ಯ ತಾಪಮಾನದಲ್ಲಿ ಅತ್ಯುತ್ತಮ ಅವಾಹಕಗಳಾಗಿವೆ, ಉದಾಹರಣೆಗೆ ಅನ್ಹೈಡ್ರಸ್ ಮೆಟಲ್ ಆಕ್ಸೈಡ್ಗಳು (ಕ್ಯಾಲ್ಸಿಯಂ ಆಕ್ಸೈಡ್, ಮೆಗ್ನೀಸಿಯಮ್ ಆಕ್ಸೈಡ್, ಇತ್ಯಾದಿ), ಮತ್ತು ತಾಪಮಾನವು ಹೆಚ್ಚಾದಾಗ ಎಲೆಕ್ಟ್ರೋಲೈಟಿಕ್ ಕಂಡಕ್ಟರ್ಗಳಾಗುತ್ತವೆ. ಪ್ರಸಿದ್ಧ ನೆರ್ನ್ಸ್ಟ್ ಪ್ರಕಾಶಮಾನ ದೀಪ, ಇದರ ತತ್ವವನ್ನು ಅದ್ಭುತ ಯಾಬ್ಲೋಚ್ಕೋವ್ ಕಂಡುಹಿಡಿದನು, ಈ ಸಂಗತಿಗಳ ಅತ್ಯುತ್ತಮ ವಿವರಣೆಯನ್ನು ಒದಗಿಸುತ್ತದೆ. ಆಕ್ಸೈಡ್ಗಳ ಮಿಶ್ರಣ - ನೆರ್ನ್ಸ್ಟ್ ದೀಪದಲ್ಲಿ "ಪ್ರಕಾಶಮಾನ ದೇಹ", ಇದು ಸಾಮಾನ್ಯ ತಾಪಮಾನದಲ್ಲಿ ವಾಹಕವಲ್ಲ, 700 ° ನಲ್ಲಿ ಅತ್ಯುತ್ತಮವಾಗುತ್ತದೆ ಮತ್ತು ಮೇಲಾಗಿ, ಘನ ಸ್ಥಿತಿಯನ್ನು ಉಳಿಸಿಕೊಳ್ಳುತ್ತದೆ. ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಕಂಡಕ್ಟರ್. ಅಜೈವಿಕ ರಸಾಯನಶಾಸ್ತ್ರದಲ್ಲಿ ಅಧ್ಯಯನ ಮಾಡಿದ ಅತ್ಯಂತ ಸಂಕೀರ್ಣ ವಸ್ತುಗಳು, ಸೂಕ್ತವಾದ ದ್ರಾವಕಗಳೊಂದಿಗೆ ಅಥವಾ ಸಾಕಷ್ಟು ಹೆಚ್ಚಿನ ತಾಪಮಾನದಲ್ಲಿ, ಲೋಹಗಳು ಮತ್ತು ಅವುಗಳ ಮಿಶ್ರಲೋಹಗಳು ಮತ್ತು ಲೋಹೀಯ ವಾಹಕತೆಯನ್ನು ಹೊಂದಿರುವ ಸಂಕೀರ್ಣ ಪದಾರ್ಥಗಳನ್ನು ಹೊರತುಪಡಿಸಿ, ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ಗುಣಲಕ್ಷಣಗಳನ್ನು ಪಡೆಯಬಹುದು ಎಂದು ಊಹಿಸಬಹುದು. ಸಾಬೀತಾಗಿದೆ. ಈ ಸಮಯದಲ್ಲಿ, ಕರಗಿದ ಸಿಲ್ವರ್ ಅಯೋಡೈಡ್, ಇತ್ಯಾದಿಗಳ ಲೋಹೀಯ ವಾಹಕತೆಯ ಸೂಚನೆಗಳನ್ನು ಇನ್ನೂ ಸಾಕಷ್ಟು ಸಮರ್ಥಿಸಲಾಗಿಲ್ಲ ಎಂದು ಪರಿಗಣಿಸಬೇಕು. ಇಂಗಾಲವನ್ನು ಹೊಂದಿರುವ ಹೆಚ್ಚಿನ ಪದಾರ್ಥಗಳ ಬಗ್ಗೆ ಬೇರೆ ಯಾವುದನ್ನಾದರೂ ಹೇಳಬೇಕು, ಅಂದರೆ, ಸಾವಯವ ರಸಾಯನಶಾಸ್ತ್ರದಲ್ಲಿ ಅಧ್ಯಯನ ಮಾಡಲಾದವುಗಳು. ಹೈಡ್ರೋಕಾರ್ಬನ್ಗಳು ಅಥವಾ ಅವುಗಳ ಮಿಶ್ರಣಗಳನ್ನು (ಪ್ಯಾರಾಫಿನ್, ಸೀಮೆಎಣ್ಣೆ, ಗ್ಯಾಸೋಲಿನ್, ಇತ್ಯಾದಿ) ಪ್ರಸ್ತುತದ ವಾಹಕಗಳನ್ನು ಮಾಡುವ ದ್ರಾವಕಗಳು ಇರುವುದು ಅಸಂಭವವಾಗಿದೆ. ಆದಾಗ್ಯೂ, ಸಾವಯವ ರಸಾಯನಶಾಸ್ತ್ರದಲ್ಲಿ ನಾವು ವಿಶಿಷ್ಟವಾದ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳಿಂದ ವಿಶಿಷ್ಟವಲ್ಲದ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳಿಗೆ ಕ್ರಮೇಣ ಪರಿವರ್ತನೆಯನ್ನು ಹೊಂದಿದ್ದೇವೆ: ಸಾವಯವ ಆಮ್ಲಗಳಿಂದ ಪ್ರಾರಂಭಿಸಿ ನೈಟ್ರೊ ಗುಂಪನ್ನು ಹೊಂದಿರುವ ಫೀನಾಲ್ಗಳಿಗೆ, ಅಂತಹ ಗುಂಪನ್ನು ಹೊಂದಿರದ ಫೀನಾಲ್ಗಳಿಗೆ, ಆಲ್ಕೋಹಾಲ್ಗಳಿಗೆ, ಜಲೀಯ ದ್ರಾವಣಗಳು ಕಡಿಮೆ ಇರುವ ಅವಾಹಕಗಳಿಗೆ ಸೇರಿವೆ. ವಿದ್ಯುತ್ ಉತ್ತೇಜಕ ಶಕ್ತಿಗಳು ಮತ್ತು , ಅಂತಿಮವಾಗಿ, ಹೈಡ್ರೋಕಾರ್ಬನ್ಗಳಿಗೆ - ವಿಶಿಷ್ಟ ಅವಾಹಕಗಳು. ಅನೇಕ ಸಾವಯವ, ಮತ್ತು ಭಾಗಶಃ ಕೆಲವು ಅಜೈವಿಕ ಸಂಯುಕ್ತಗಳಿಗೆ, ತಾಪಮಾನದಲ್ಲಿನ ಹೆಚ್ಚಳವು ಅವುಗಳನ್ನು ಇ. ಮಾಡುತ್ತದೆ ಎಂದು ನಿರೀಕ್ಷಿಸುವುದು ಕಷ್ಟ, ಏಕೆಂದರೆ ಈ ವಸ್ತುಗಳು ಶಾಖದ ಕ್ರಿಯೆಯಿಂದ ಮೊದಲೇ ಕೊಳೆಯುತ್ತವೆ.
ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯ ಎಂದರೇನು ಎಂಬ ಪ್ರಶ್ನೆಯು ಅಂತಹ ಅನಿಶ್ಚಿತ ಸ್ಥಿತಿಯಲ್ಲಿತ್ತು, ಅದನ್ನು ಪರಿಹರಿಸಲು ಎಲೆಕ್ಟ್ರೋಲೈಟಿಕ್ ಡಿಸೋಸಿಯೇಶನ್ ಸಿದ್ಧಾಂತವನ್ನು ತರಲಾಯಿತು.
ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯ ವಿಘಟನೆ.
ಅಯಾನುಗಳಾಗಿ ಎಲೆಕ್ಟ್ರೋಲೈಟ್ ಅಣುಗಳ ವಿಘಟನೆಯನ್ನು ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯ ವಿಘಟನೆ ಅಥವಾ ಅಯಾನೀಕರಣ ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ ಮತ್ತು ಇದು ಹಿಂತಿರುಗಿಸಬಹುದಾದ ಪ್ರಕ್ರಿಯೆಯಾಗಿದೆ, ಅಂದರೆ, ಅನೇಕ ಎಲೆಕ್ಟ್ರೋಲೈಟ್ ಅಣುಗಳು ಅಯಾನುಗಳಾಗಿ ವಿಭಜನೆಯಾಗುವ ದ್ರಾವಣದಲ್ಲಿ ಸಮತೋಲನ ಸ್ಥಿತಿಯು ಸಂಭವಿಸಬಹುದು, ಆದ್ದರಿಂದ ಅವುಗಳಲ್ಲಿ ಹಲವು ಅಯಾನುಗಳಿಂದ ಮತ್ತೆ ರೂಪುಗೊಳ್ಳುತ್ತವೆ. .
ಅಯಾನುಗಳಾಗಿ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳ ವಿಘಟನೆಯನ್ನು ಸಾಮಾನ್ಯ ಸಮೀಕರಣದಿಂದ ಪ್ರತಿನಿಧಿಸಬಹುದು: , KmAn ಒಂದು ಬೇರ್ಪಡಿಸದ ಅಣುವಾಗಿದೆ, K z+ 1 ಎಂಬುದು z 1 ಧನಾತ್ಮಕ ಆವೇಶಗಳನ್ನು ಹೊಂದಿರುವ ಕ್ಯಾಷನ್ ಆಗಿದೆ, ಮತ್ತು z- 2 ಎಂಬುದು z 2 ಋಣಾತ್ಮಕ ಶುಲ್ಕಗಳು, m ಮತ್ತು n ಹೊಂದಿರುವ ಅಯಾನ್ ಆಗಿದೆ. ಒಂದು ಎಲೆಕ್ಟ್ರೋಲೈಟ್ ಅಣುವಿನ ವಿಘಟನೆಯ ಸಮಯದಲ್ಲಿ ರೂಪುಗೊಂಡ ಕ್ಯಾಟಯಾನುಗಳು ಮತ್ತು ಅಯಾನುಗಳ ಸಂಖ್ಯೆ. ಉದಾಹರಣೆಗೆ, .
ದ್ರಾವಣದಲ್ಲಿನ ಧನಾತ್ಮಕ ಮತ್ತು ಋಣಾತ್ಮಕ ಅಯಾನುಗಳ ಸಂಖ್ಯೆಯು ವಿಭಿನ್ನವಾಗಿರಬಹುದು, ಆದರೆ ಕ್ಯಾಟಯಾನುಗಳ ಒಟ್ಟು ಚಾರ್ಜ್ ಯಾವಾಗಲೂ ಅಯಾನುಗಳ ಒಟ್ಟು ಚಾರ್ಜ್ಗೆ ಸಮಾನವಾಗಿರುತ್ತದೆ, ಆದ್ದರಿಂದ ಒಟ್ಟಾರೆಯಾಗಿ ಪರಿಹಾರವು ವಿದ್ಯುತ್ ತಟಸ್ಥವಾಗಿರುತ್ತದೆ.
ಬಲವಾದ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳು ದ್ರಾವಣದಲ್ಲಿ ಯಾವುದೇ ಸಾಂದ್ರತೆಯಲ್ಲಿ ಅಯಾನುಗಳಾಗಿ ಸಂಪೂರ್ಣವಾಗಿ ವಿಭಜನೆಗೊಳ್ಳುತ್ತವೆ. ಇವುಗಳಲ್ಲಿ ಬಲವಾದ ಆಮ್ಲಗಳು (ನೋಡಿ), ಬಲವಾದ ಬೇಸ್ಗಳು ಮತ್ತು ಬಹುತೇಕ ಎಲ್ಲಾ ಲವಣಗಳು (ನೋಡಿ) ಸೇರಿವೆ. ದುರ್ಬಲವಾದ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳು, ಇದರಲ್ಲಿ ದುರ್ಬಲ ಆಮ್ಲಗಳು ಮತ್ತು ಬೇಸ್ಗಳು ಮತ್ತು ಕೆಲವು ಲವಣಗಳು, ಉದಾಹರಣೆಗೆ ಸಬ್ಲೈಮೇಟ್ HgCl 2, ಭಾಗಶಃ ಮಾತ್ರ ವಿಭಜನೆಯಾಗುತ್ತವೆ; ಅವುಗಳ ವಿಘಟನೆಯ ಮಟ್ಟ, ಅಂದರೆ, ಅಯಾನುಗಳಾಗಿ ವಿಭಜನೆಯಾದ ಅಣುಗಳ ಪ್ರಮಾಣವು ದ್ರಾವಣದ ಸಾಂದ್ರತೆಯು ಕಡಿಮೆಯಾಗುವುದರೊಂದಿಗೆ ಹೆಚ್ಚಾಗುತ್ತದೆ.
ದ್ರಾವಣಗಳಲ್ಲಿ ಅಯಾನುಗಳಾಗಿ ವಿಘಟನೆಯಾಗುವ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳ ಸಾಮರ್ಥ್ಯದ ಅಳತೆಯು ಎಲೆಕ್ಟ್ರೋಲೈಟಿಕ್ ಡಿಸೋಸಿಯೇಷನ್ ಸ್ಥಿರ (ಅಯಾನೀಕರಣ ಸ್ಥಿರ) ಆಗಿರಬಹುದು
ಅಲ್ಲಿ ದ್ರಾವಣದಲ್ಲಿನ ಅನುಗುಣವಾದ ಕಣಗಳ ಸಾಂದ್ರತೆಯನ್ನು ಚದರ ಆವರಣಗಳಲ್ಲಿ ತೋರಿಸಲಾಗುತ್ತದೆ.
1. ಎಲೆಕ್ಟ್ರೋಲೈಟ್ಗಳು
1.1. ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯ ವಿಘಟನೆ. ವಿಘಟನೆಯ ಪದವಿ. ಎಲೆಕ್ಟ್ರೋಲೈಟ್ ಪವರ್
ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯ ವಿಘಟನೆಯ ಸಿದ್ಧಾಂತದ ಪ್ರಕಾರ, ಲವಣಗಳು, ಆಮ್ಲಗಳು, ಹೈಡ್ರಾಕ್ಸೈಡ್ಗಳು, ನೀರಿನಲ್ಲಿ ಕರಗುವಿಕೆ, ಸಂಪೂರ್ಣವಾಗಿ ಅಥವಾ ಭಾಗಶಃ ಸ್ವತಂತ್ರ ಕಣಗಳಾಗಿ ವಿಭಜನೆಯಾಗುತ್ತವೆ - ಅಯಾನುಗಳು.
ಧ್ರುವೀಯ ದ್ರಾವಕ ಅಣುಗಳ ಪ್ರಭಾವದ ಅಡಿಯಲ್ಲಿ ವಸ್ತುವಿನ ಅಣುಗಳನ್ನು ಅಯಾನುಗಳಾಗಿ ವಿಭಜಿಸುವ ಪ್ರಕ್ರಿಯೆಯನ್ನು ಎಲೆಕ್ಟ್ರೋಲೈಟಿಕ್ ಡಿಸೋಸಿಯೇಷನ್ ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ. ದ್ರಾವಣಗಳಲ್ಲಿ ಅಯಾನುಗಳಾಗಿ ವಿಭಜನೆಯಾಗುವ ಪದಾರ್ಥಗಳನ್ನು ಕರೆಯಲಾಗುತ್ತದೆ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳು.ಪರಿಣಾಮವಾಗಿ, ಪರಿಹಾರವು ವಿದ್ಯುತ್ ಪ್ರವಾಹವನ್ನು ನಡೆಸುವ ಸಾಮರ್ಥ್ಯವನ್ನು ಪಡೆಯುತ್ತದೆ, ಏಕೆಂದರೆ ಮೊಬೈಲ್ ಎಲೆಕ್ಟ್ರಿಕ್ ಚಾರ್ಜ್ ಕ್ಯಾರಿಯರ್ಗಳು ಅದರಲ್ಲಿ ಕಾಣಿಸಿಕೊಳ್ಳುತ್ತವೆ. ಈ ಸಿದ್ಧಾಂತದ ಪ್ರಕಾರ, ನೀರಿನಲ್ಲಿ ಕರಗಿದಾಗ, ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳು ಧನಾತ್ಮಕ ಮತ್ತು ಋಣಾತ್ಮಕ ಆವೇಶದ ಅಯಾನುಗಳಾಗಿ ಒಡೆಯುತ್ತವೆ (ಬೇರ್ಪಡುತ್ತವೆ). ಧನಾತ್ಮಕ ಆವೇಶದ ಅಯಾನುಗಳನ್ನು ಕರೆಯಲಾಗುತ್ತದೆ ಕ್ಯಾಟಯಾನುಗಳು; ಇವುಗಳಲ್ಲಿ, ಉದಾಹರಣೆಗೆ, ಹೈಡ್ರೋಜನ್ ಮತ್ತು ಲೋಹದ ಅಯಾನುಗಳು ಸೇರಿವೆ. ಋಣಾತ್ಮಕ ಚಾರ್ಜ್ಡ್ ಅಯಾನುಗಳನ್ನು ಕರೆಯಲಾಗುತ್ತದೆ ಅಯಾನುಗಳು; ಇವುಗಳಲ್ಲಿ ಆಮ್ಲೀಯ ಉಳಿಕೆಗಳು ಮತ್ತು ಹೈಡ್ರಾಕ್ಸೈಡ್ ಅಯಾನುಗಳ ಅಯಾನುಗಳು ಸೇರಿವೆ.
ವಿಘಟನೆಯ ಪ್ರಕ್ರಿಯೆಯನ್ನು ಪರಿಮಾಣಾತ್ಮಕವಾಗಿ ನಿರೂಪಿಸಲು, ವಿಘಟನೆಯ ಪದವಿಯ ಪರಿಕಲ್ಪನೆಯನ್ನು ಪರಿಚಯಿಸಲಾಯಿತು. ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯದ (α) ವಿಘಟನೆಯ ಮಟ್ಟವು ನಿರ್ದಿಷ್ಟ ದ್ರಾವಣದಲ್ಲಿ ಅಯಾನುಗಳಾಗಿ ವಿಭಜನೆಯಾದ ಅದರ ಅಣುಗಳ ಸಂಖ್ಯೆಯ ಅನುಪಾತವಾಗಿದೆ (ಎನ್ ), ದ್ರಾವಣದಲ್ಲಿರುವ ಅದರ ಅಣುಗಳ ಒಟ್ಟು ಸಂಖ್ಯೆಗೆ (ಎನ್), ಅಥವಾ
α = .
ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯದ ವಿಘಟನೆಯ ಮಟ್ಟವನ್ನು ಸಾಮಾನ್ಯವಾಗಿ ಒಂದು ಘಟಕದ ಭಿನ್ನರಾಶಿಗಳಲ್ಲಿ ಅಥವಾ ಶೇಕಡಾವಾರು ಪ್ರಮಾಣದಲ್ಲಿ ವ್ಯಕ್ತಪಡಿಸಲಾಗುತ್ತದೆ.
0.3 (30%) ಕ್ಕಿಂತ ಹೆಚ್ಚಿನ ವಿಘಟನೆಯ ಮಟ್ಟವನ್ನು ಹೊಂದಿರುವ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳನ್ನು ಸಾಮಾನ್ಯವಾಗಿ ಪ್ರಬಲ ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ, 0.03 (3%) ನಿಂದ 0.3 (30%) ವರೆಗಿನ ವಿಘಟನೆಯ ಪದವಿಯೊಂದಿಗೆ - ಮಧ್ಯಮ, 0.03 ಕ್ಕಿಂತ ಕಡಿಮೆ (3%) - ದುರ್ಬಲ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳು. ಆದ್ದರಿಂದ, 0.1 M ಪರಿಹಾರಕ್ಕಾಗಿ CH3COOH α = 0.013 (ಅಥವಾ 1.3%). ಆದ್ದರಿಂದ, ಅಸಿಟಿಕ್ ಆಮ್ಲವು ದುರ್ಬಲ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯವಾಗಿದೆ. ವಿಘಟನೆಯ ಮಟ್ಟವು ವಸ್ತುವಿನ ಕರಗಿದ ಅಣುಗಳ ಯಾವ ಭಾಗವು ಅಯಾನುಗಳಾಗಿ ವಿಭಜನೆಯಾಗಿದೆ ಎಂಬುದನ್ನು ತೋರಿಸುತ್ತದೆ. ಜಲೀಯ ದ್ರಾವಣಗಳಲ್ಲಿ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯದ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯದ ವಿಘಟನೆಯ ಮಟ್ಟವು ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯದ ಸ್ವರೂಪ, ಅದರ ಸಾಂದ್ರತೆ ಮತ್ತು ತಾಪಮಾನವನ್ನು ಅವಲಂಬಿಸಿರುತ್ತದೆ.
ಅವುಗಳ ಸ್ವಭಾವದಿಂದ, ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳನ್ನು ಎರಡು ದೊಡ್ಡ ಗುಂಪುಗಳಾಗಿ ವಿಂಗಡಿಸಬಹುದು: ಬಲವಾದ ಮತ್ತು ದುರ್ಬಲ. ಬಲವಾದ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳುಬಹುತೇಕ ಸಂಪೂರ್ಣವಾಗಿ ಬೇರ್ಪಡಿಸಿ (α = 1).
ಬಲವಾದ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳು ಸೇರಿವೆ:
1) ಆಮ್ಲಗಳು (H 2 SO 4, HCl, HNO 3, HBr, HI, HClO 4, H M nO 4);
2) ಬೇಸ್ಗಳು - ಮುಖ್ಯ ಉಪಗುಂಪಿನ (ಕ್ಷಾರ) ಮೊದಲ ಗುಂಪಿನ ಲೋಹದ ಹೈಡ್ರಾಕ್ಸೈಡ್ಗಳು - LiOH, NaOH, KOH, RbOH, CsOH , ಹಾಗೆಯೇ ಕ್ಷಾರೀಯ ಭೂಮಿಯ ಲೋಹಗಳ ಹೈಡ್ರಾಕ್ಸೈಡ್ಗಳು - Ba (OH) 2, Ca (OH) 2, Sr (OH) 2;.
3) ನೀರಿನಲ್ಲಿ ಕರಗುವ ಲವಣಗಳು (ಕರಗುವ ಕೋಷ್ಟಕವನ್ನು ನೋಡಿ).
ದುರ್ಬಲ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳು ಬಹಳ ಕಡಿಮೆ ಪ್ರಮಾಣದಲ್ಲಿ ಅಯಾನುಗಳಾಗಿ ವಿಭಜನೆಯಾಗುತ್ತವೆ; ದುರ್ಬಲ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳಿಗೆ, ಬೇರ್ಪಡಿಸದ ಅಣುಗಳು ಮತ್ತು ಅಯಾನುಗಳ ನಡುವೆ ಸಮತೋಲನವನ್ನು ಸ್ಥಾಪಿಸಲಾಗಿದೆ.
ದುರ್ಬಲ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳು ಸೇರಿವೆ:
1) ಅಜೈವಿಕ ಆಮ್ಲಗಳು ( H 2 CO 3, H 2 S, HNO 2, H 2 SO 3, HCN, H 3 PO 4, H 2 SiO 3, HCNS, HClO, ಇತ್ಯಾದಿ);
2) ನೀರು (H 2 O);
3) ಅಮೋನಿಯಂ ಹೈಡ್ರಾಕ್ಸೈಡ್ ( NH 4 OH);
4) ಹೆಚ್ಚಿನ ಸಾವಯವ ಆಮ್ಲಗಳು
(ಉದಾಹರಣೆಗೆ, ಅಸಿಟಿಕ್ CH 3 COOH, ಫಾರ್ಮಿಕ್ HCOOH);
5) ಕರಗದ ಮತ್ತು ಸ್ವಲ್ಪ ಕರಗುವ ಲವಣಗಳು ಮತ್ತು ಕೆಲವು ಲೋಹಗಳ ಹೈಡ್ರಾಕ್ಸೈಡ್ಗಳು (ಕರಗುವ ಕೋಷ್ಟಕವನ್ನು ನೋಡಿ).
ಪ್ರಕ್ರಿಯೆ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯ ವಿಘಟನೆರಾಸಾಯನಿಕ ಸಮೀಕರಣಗಳನ್ನು ಬಳಸಿ ಚಿತ್ರಿಸಲಾಗಿದೆ. ಉದಾಹರಣೆಗೆ, ಹೈಡ್ರೋಕ್ಲೋರಿಕ್ ಆಮ್ಲದ ವಿಘಟನೆ (HCಎಲ್ ) ಈ ಕೆಳಗಿನಂತೆ ಬರೆಯಲಾಗಿದೆ:
HCl → H + + Cl – .
ಲೋಹದ ಕ್ಯಾಟಯಾನುಗಳು ಮತ್ತು ಹೈಡ್ರಾಕ್ಸೈಡ್ ಅಯಾನುಗಳನ್ನು ರೂಪಿಸಲು ಬೇಸ್ಗಳು ವಿಭಜನೆಗೊಳ್ಳುತ್ತವೆ. ಉದಾಹರಣೆಗೆ, KOH ನ ವಿಘಟನೆ
KOH → K + + OH - .
ಪಾಲಿಬಾಸಿಕ್ ಆಮ್ಲಗಳು, ಹಾಗೆಯೇ ಪಾಲಿವೇಲೆಂಟ್ ಲೋಹಗಳ ಬೇಸ್ಗಳು ಹಂತಹಂತವಾಗಿ ವಿಯೋಜಿಸುತ್ತವೆ. ಉದಾಹರಣೆಗೆ,
H 2 CO 3 H + + HCO 3 – ,
HCO 3 – H + + CO 3 2– .
ಮೊದಲ ಸಮತೋಲನ - ಮೊದಲ ಹಂತದ ಪ್ರಕಾರ ವಿಘಟನೆ - ಸ್ಥಿರತೆಯಿಂದ ನಿರೂಪಿಸಲ್ಪಟ್ಟಿದೆ
![]() .
.
ಎರಡನೇ ಹಂತದ ವಿಭಜನೆಗಾಗಿ:
![]() .
.
ಕಾರ್ಬೊನಿಕ್ ಆಮ್ಲದ ಸಂದರ್ಭದಲ್ಲಿ, ವಿಘಟನೆಯ ಸ್ಥಿರಾಂಕಗಳು ಈ ಕೆಳಗಿನ ಮೌಲ್ಯಗಳನ್ನು ಹೊಂದಿವೆ: ಕೆ I = 4.3× 10 -7, ಕೆ II = 5.6 × 10–11. ಯಾವಾಗಲೂ ಹಂತ ಹಂತವಾಗಿ ವಿಘಟನೆಗಾಗಿ ಕೆ I> ಕೆ II > ಕೆ III >... , ಏಕೆಂದರೆ ತಟಸ್ಥ ಅಣುವಿನಿಂದ ಬೇರ್ಪಡಿಸಿದಾಗ ಅಯಾನನ್ನು ಬೇರ್ಪಡಿಸಲು ವ್ಯಯಿಸಬೇಕಾದ ಶಕ್ತಿಯು ಕಡಿಮೆಯಿರುತ್ತದೆ.
ಸರಾಸರಿ (ಸಾಮಾನ್ಯ) ಲವಣಗಳು, ನೀರಿನಲ್ಲಿ ಕರಗುತ್ತವೆ, ಧನಾತ್ಮಕ ಆವೇಶದ ಲೋಹದ ಅಯಾನುಗಳು ಮತ್ತು ಆಮ್ಲ ಶೇಷದ ಋಣಾತ್ಮಕ ಆವೇಶದ ಅಯಾನುಗಳನ್ನು ರೂಪಿಸಲು ವಿಘಟಿಸುತ್ತವೆ.
Ca(NO 3) 2 → Ca 2+ + 2NO 3 –
ಅಲ್ 2 (SO 4) 3 → 2Al 3+ +3SO 4 2–.
ಆಮ್ಲ ಲವಣಗಳು (ಹೈಡ್ರೋಸಾಲ್ಟ್ಗಳು) ಅಯಾನುಗಳಲ್ಲಿ ಹೈಡ್ರೋಜನ್ ಅನ್ನು ಒಳಗೊಂಡಿರುವ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳಾಗಿವೆ, ಇದನ್ನು ಹೈಡ್ರೋಜನ್ ಅಯಾನು H + ರೂಪದಲ್ಲಿ ವಿಭಜಿಸಬಹುದು. ಆಮ್ಲ ಲವಣಗಳನ್ನು ಪಾಲಿಬಾಸಿಕ್ ಆಮ್ಲಗಳಿಂದ ಪಡೆದ ಉತ್ಪನ್ನವೆಂದು ಪರಿಗಣಿಸಲಾಗುತ್ತದೆ, ಇದರಲ್ಲಿ ಎಲ್ಲಾ ಹೈಡ್ರೋಜನ್ ಪರಮಾಣುಗಳನ್ನು ಲೋಹದಿಂದ ಬದಲಾಯಿಸಲಾಗುವುದಿಲ್ಲ. ಆಮ್ಲ ಲವಣಗಳ ವಿಘಟನೆಯು ಹಂತಗಳಲ್ಲಿ ಸಂಭವಿಸುತ್ತದೆ, ಉದಾಹರಣೆಗೆ:
KHCO 3 → K + + HCO 3 - (ಮೊದಲ ಹಂತ)
ಎಲೆಕ್ಟ್ರೋಲೈಟ್ಗಳು ಕರಗುವ ಅಥವಾ ದ್ರಾವಣಗಳು ವಿದ್ಯುತ್ ಪ್ರವಾಹವನ್ನು ನಡೆಸುವ ಪದಾರ್ಥಗಳಾಗಿವೆ. ಎಲೆಕ್ಟ್ರೋಲೈಟ್ಗಳು ಆಮ್ಲಗಳು, ಬೇಸ್ಗಳು ಮತ್ತು ಹೆಚ್ಚಿನ ಲವಣಗಳನ್ನು ಒಳಗೊಂಡಿರುತ್ತವೆ.
ಎಲೆಕ್ಟ್ರೋಲೈಟ್ ವಿಘಟನೆ
ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳು ಅಯಾನಿಕ್ ಅಥವಾ ಹೆಚ್ಚು ಧ್ರುವೀಯ ಕೋವೆಲನ್ಸಿಯ ಬಂಧಗಳೊಂದಿಗೆ ಪದಾರ್ಥಗಳನ್ನು ಒಳಗೊಂಡಿರುತ್ತವೆ. ಮೊದಲಿನವುಗಳು ಕರಗಿದ ಅಥವಾ ಕರಗಿದ ಸ್ಥಿತಿಗೆ ವರ್ಗಾವಣೆಯಾಗುವ ಮೊದಲೇ ಅಯಾನುಗಳ ರೂಪದಲ್ಲಿ ಅಸ್ತಿತ್ವದಲ್ಲಿವೆ. ಎಲೆಕ್ಟ್ರೋಲೈಟ್ಗಳು ಲವಣಗಳು, ಬೇಸ್ಗಳು ಮತ್ತು ಆಮ್ಲಗಳನ್ನು ಒಳಗೊಂಡಿರುತ್ತವೆ.

ಅಕ್ಕಿ. 1. ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳು ಮತ್ತು ನಾನ್-ಎಲೆಕ್ಟ್ರೋಲೈಟ್ಗಳ ನಡುವಿನ ವ್ಯತ್ಯಾಸವನ್ನು ಟೇಬಲ್ ಮಾಡಿ.
ಬಲವಾದ ಮತ್ತು ದುರ್ಬಲ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳಿವೆ. ಬಲವಾದ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳು, ನೀರಿನಲ್ಲಿ ಕರಗಿದಾಗ, ಸಂಪೂರ್ಣವಾಗಿ ಅಯಾನುಗಳಾಗಿ ವಿಭಜಿಸುತ್ತವೆ. ಅವುಗಳೆಂದರೆ: ಬಹುತೇಕ ಎಲ್ಲಾ ಕರಗುವ ಲವಣಗಳು, ಅನೇಕ ಅಜೈವಿಕ ಆಮ್ಲಗಳು (ಉದಾಹರಣೆಗೆ, H 2 SO 4, HNO 3, HCl), ಕ್ಷಾರ ಮತ್ತು ಕ್ಷಾರೀಯ ಭೂಮಿಯ ಲೋಹಗಳ ಹೈಡ್ರಾಕ್ಸೈಡ್ಗಳು. ದುರ್ಬಲ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳು, ನೀರಿನಲ್ಲಿ ಕರಗಿದಾಗ, ಸ್ವಲ್ಪಮಟ್ಟಿಗೆ ಅಯಾನುಗಳಾಗಿ ವಿಭಜನೆಯಾಗುತ್ತವೆ. ಇವುಗಳಲ್ಲಿ ಬಹುತೇಕ ಎಲ್ಲಾ ಸಾವಯವ ಆಮ್ಲಗಳು, ಕೆಲವು ಅಜೈವಿಕ ಆಮ್ಲಗಳು (ಉದಾಹರಣೆಗೆ, H 2 CO 3), ಅನೇಕ ಹೈಡ್ರಾಕ್ಸೈಡ್ಗಳು (ಕ್ಷಾರ ಮತ್ತು ಕ್ಷಾರೀಯ ಭೂಮಿಯ ಲೋಹಗಳ ಹೈಡ್ರಾಕ್ಸೈಡ್ಗಳನ್ನು ಹೊರತುಪಡಿಸಿ).

ಅಕ್ಕಿ. 2. ಬಲವಾದ ಮತ್ತು ದುರ್ಬಲ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳ ಟೇಬಲ್.
ನೀರು ಕೂಡ ದುರ್ಬಲ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯವಾಗಿದೆ.
ಇತರ ರಾಸಾಯನಿಕ ಕ್ರಿಯೆಗಳಂತೆ, ದ್ರಾವಣಗಳಲ್ಲಿ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯ ವಿಘಟನೆಯನ್ನು ವಿಘಟನೆಯ ಸಮೀಕರಣಗಳ ರೂಪದಲ್ಲಿ ಬರೆಯಲಾಗುತ್ತದೆ. ಅದೇ ಸಮಯದಲ್ಲಿ, ಬಲವಾದ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳಿಗೆ ಪ್ರಕ್ರಿಯೆಯನ್ನು ಬದಲಾಯಿಸಲಾಗದು ಎಂದು ಪರಿಗಣಿಸಲಾಗುತ್ತದೆ ಮತ್ತು ಮಧ್ಯಮ ಶಕ್ತಿ ಮತ್ತು ದುರ್ಬಲ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳಿಗೆ - ಹಿಂತಿರುಗಿಸಬಹುದಾದ ಪ್ರಕ್ರಿಯೆಯಾಗಿ.
ಆಮ್ಲಗಳು- ಇವು ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳು, ಜಲೀಯ ದ್ರಾವಣಗಳಲ್ಲಿ ವಿಘಟನೆಯು ಕ್ಯಾಟಯಾನುಗಳಾಗಿ ಹೈಡ್ರೋಜನ್ ಅಯಾನುಗಳ ರಚನೆಯೊಂದಿಗೆ ಸಂಭವಿಸುತ್ತದೆ. ಪಾಲಿಬಾಸಿಕ್ ಆಮ್ಲಗಳು ಹಂತಹಂತವಾಗಿ ವಿಭಜನೆಗೊಳ್ಳುತ್ತವೆ. ಪ್ರತಿ ನಂತರದ ಹಂತವು ಹೆಚ್ಚಿನ ಮತ್ತು ಹೆಚ್ಚಿನ ಕಷ್ಟದಿಂದ ಮುಂದುವರಿಯುತ್ತದೆ, ಏಕೆಂದರೆ ಆಮ್ಲೀಯ ಶೇಷಗಳ ಅಯಾನುಗಳು ದುರ್ಬಲ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳಾಗಿವೆ.
ಮೈದಾನಗಳು- ಹೈಡ್ರಾಕ್ಸೈಡ್ ಅಯಾನು OH- ಅನ್ನು ಅಯಾನ್ ಆಗಿ ರೂಪಿಸಲು ಜಲೀಯ ದ್ರಾವಣದಲ್ಲಿ ವಿಯೋಜಿಸುವ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳು. ಹೈಡ್ರಾಕ್ಸೈಡ್ ಅಯಾನಿನ ರಚನೆಯು ಬೇಸ್ಗಳ ಸಾಮಾನ್ಯ ಲಕ್ಷಣವಾಗಿದೆ ಮತ್ತು ಬಲವಾದ ನೆಲೆಗಳ ಸಾಮಾನ್ಯ ಗುಣಲಕ್ಷಣಗಳನ್ನು ನಿರ್ಧರಿಸುತ್ತದೆ: ಕ್ಷಾರೀಯ ಪಾತ್ರ, ಕಹಿ ರುಚಿ, ಸ್ಪರ್ಶಕ್ಕೆ ಸಾಬೂನು, ಸೂಚಕಕ್ಕೆ ಪ್ರತಿಕ್ರಿಯೆ, ಆಮ್ಲಗಳ ತಟಸ್ಥೀಕರಣ, ಇತ್ಯಾದಿ.
ಕ್ಷಾರಗಳು, ಸ್ವಲ್ಪ ಕರಗಬಲ್ಲವುಗಳು (ಉದಾಹರಣೆಗೆ, ಬೇರಿಯಮ್ ಹೈಡ್ರಾಕ್ಸೈಡ್ Ba(OH) 2) ಸಂಪೂರ್ಣವಾಗಿ ವಿಭಜನೆಯಾಗುತ್ತದೆ, ಉದಾಹರಣೆಗೆ:
Ba(OH) 2 =Ba 2 +2OH-
ಲವಣಗಳುಲೋಹದ ಕ್ಯಾಷನ್ ಮತ್ತು ಆಮ್ಲದ ಶೇಷವನ್ನು ರೂಪಿಸಲು ಜಲೀಯ ದ್ರಾವಣದಲ್ಲಿ ಬೇರ್ಪಡಿಸುವ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳಾಗಿವೆ. ಲವಣಗಳು ಹಂತ ಹಂತವಾಗಿ ವಿಭಜನೆಯಾಗುವುದಿಲ್ಲ, ಆದರೆ ಸಂಪೂರ್ಣವಾಗಿ:
Сa(NO 3) 2 =Ca 2 + +2NO 3 -
ಎಲೆಕ್ಟ್ರೋಲೈಟಿಕ್ ಡಿಸೋಸಿಯೇಷನ್ ಸಿದ್ಧಾಂತ
ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳು- ಅಯಾನುಗಳ ಚಲನೆಯಿಂದಾಗಿ ದ್ರಾವಣಗಳಲ್ಲಿ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯ ವಿಘಟನೆಗೆ ಒಳಗಾಗುವ ಅಥವಾ ಕರಗುವ ಮತ್ತು ವಿದ್ಯುತ್ ಪ್ರವಾಹವನ್ನು ನಡೆಸುವ ವಸ್ತುಗಳು.
ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯ ವಿಘಟನೆಯು ನೀರಿನಲ್ಲಿ ಕರಗಿದಾಗ ಅಯಾನುಗಳಾಗಿ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳ ವಿಭಜನೆಯಾಗಿದೆ.
ಆಧುನಿಕ ತಿಳುವಳಿಕೆಯಲ್ಲಿ ಎಲೆಕ್ಟ್ರೋಲೈಟಿಕ್ ಡಿಸೋಸಿಯೇಷನ್ (S. ಅರ್ಹೆನಿಯಸ್, 1887) ಸಿದ್ಧಾಂತವು ಈ ಕೆಳಗಿನ ನಿಬಂಧನೆಗಳನ್ನು ಒಳಗೊಂಡಿದೆ:
- ನೀರಿನಲ್ಲಿ ಕರಗಿದಾಗ, ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳು ಅಯಾನುಗಳಾಗಿ ವಿಭಜಿಸುತ್ತವೆ (ವಿಯೋಜನೆ) - ಧನಾತ್ಮಕ (ಕ್ಯಾಟಯಾನ್ಸ್) ಮತ್ತು ಋಣಾತ್ಮಕ (ಆಯಾನುಗಳು). ಅಯಾನಿಕ್ ಬಂಧಗಳೊಂದಿಗೆ (ಲವಣಗಳು, ಕ್ಷಾರಗಳು) ಸಂಯುಕ್ತಗಳಿಗೆ ಅಯಾನೀಕರಣವು ಅತ್ಯಂತ ಸುಲಭವಾಗಿ ಸಂಭವಿಸುತ್ತದೆ, ಇದು ಕರಗಿದಾಗ (ಸ್ಫಟಿಕ ಜಾಲರಿಯ ನಾಶದ ಎಂಡೋಥರ್ಮಿಕ್ ಪ್ರಕ್ರಿಯೆ), ಹೈಡ್ರೀಕರಿಸಿದ ಅಯಾನುಗಳನ್ನು ರೂಪಿಸುತ್ತದೆ.

ಅಕ್ಕಿ. 3. ಉಪ್ಪಿನ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯ ವಿಯೋಜನೆಯ ಯೋಜನೆ.
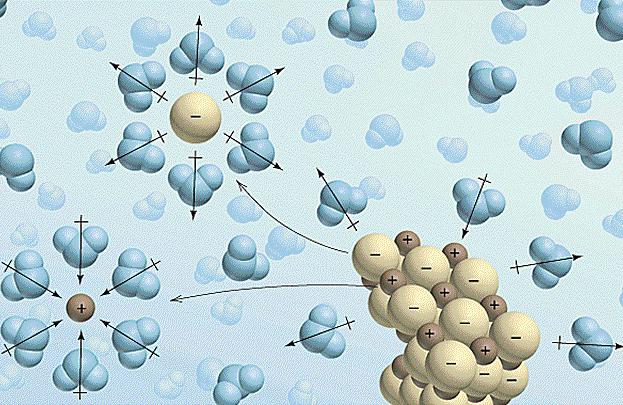
ಅಯಾನು ಜಲಸಂಚಯನವು ಎಕ್ಸೋಥರ್ಮಿಕ್ ಪ್ರಕ್ರಿಯೆಯಾಗಿದೆ. ಶಕ್ತಿಯ ವೆಚ್ಚಗಳು ಮತ್ತು ಲಾಭಗಳ ಅನುಪಾತವು ದ್ರಾವಣದಲ್ಲಿ ಅಯಾನೀಕರಣದ ಸಾಧ್ಯತೆಯನ್ನು ನಿರ್ಧರಿಸುತ್ತದೆ. ಧ್ರುವೀಯ ಕೋವೆಲನ್ಸಿಯ ಬಂಧವನ್ನು ಹೊಂದಿರುವ ವಸ್ತುವನ್ನು (ಉದಾಹರಣೆಗೆ, ಹೈಡ್ರೋಜನ್ ಕ್ಲೋರೈಡ್ HCl) ಕರಗಿಸಿದಾಗ, ನೀರಿನ ದ್ವಿಧ್ರುವಿಗಳು ಕರಗಿದ ಅಣುವಿನ ಅನುಗುಣವಾದ ಧ್ರುವಗಳಲ್ಲಿ ಆಧಾರಿತವಾಗಿರುತ್ತವೆ, ಬಂಧವನ್ನು ಧ್ರುವೀಕರಿಸುತ್ತದೆ ಮತ್ತು ಅದನ್ನು ಅಯಾನಿಕ್ ಆಗಿ ಪರಿವರ್ತಿಸುತ್ತದೆ, ನಂತರ ಅಯಾನುಗಳ ಜಲಸಂಚಯನವಾಗುತ್ತದೆ. . ಈ ಪ್ರಕ್ರಿಯೆಯು ಹಿಂತಿರುಗಿಸಬಲ್ಲದು ಮತ್ತು ಸಂಪೂರ್ಣವಾಗಿ ಅಥವಾ ಭಾಗಶಃ ಸಂಭವಿಸಬಹುದು.
- ಹೈಡ್ರೀಕರಿಸಿದ ಅಯಾನುಗಳು ಸ್ಥಿರವಾಗಿರುತ್ತವೆ ಮತ್ತು ದ್ರಾವಣದಲ್ಲಿ ಯಾದೃಚ್ಛಿಕವಾಗಿ ಚಲಿಸುತ್ತವೆ. ವಿದ್ಯುತ್ ಪ್ರವಾಹದ ಪ್ರಭಾವದ ಅಡಿಯಲ್ಲಿ, ಚಲನೆಯು ದಿಕ್ಕಿನಂತಾಗುತ್ತದೆ: ಕ್ಯಾಟಯಾನುಗಳು ಋಣಾತ್ಮಕ ಬೆಲ್ಟ್ (ಕ್ಯಾಥೋಡ್) ಕಡೆಗೆ ಚಲಿಸುತ್ತವೆ, ಮತ್ತು ಅಯಾನುಗಳು ಧನಾತ್ಮಕ ಬೆಲ್ಟ್ (ಆನೋಡ್) ಕಡೆಗೆ ಚಲಿಸುತ್ತವೆ.
- ವಿಘಟನೆ (ಅಯಾನೀಕರಣ) ಒಂದು ಹಿಮ್ಮುಖ ಪ್ರಕ್ರಿಯೆಯಾಗಿದೆ. ಅಯಾನೀಕರಣದ ಸಂಪೂರ್ಣತೆಯು ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯದ ಸ್ವರೂಪವನ್ನು ಅವಲಂಬಿಸಿರುತ್ತದೆ (ಕ್ಷಾರ ಲವಣಗಳು ಬಹುತೇಕ ಸಂಪೂರ್ಣವಾಗಿ ವಿಭಜನೆಯಾಗುತ್ತವೆ), ಅದರ ಸಾಂದ್ರತೆ (ಹೆಚ್ಚುತ್ತಿರುವ ಸಾಂದ್ರತೆಯೊಂದಿಗೆ, ಅಯಾನೀಕರಣವು ಹೆಚ್ಚು ಕಷ್ಟಕರವಾಗುತ್ತದೆ), ತಾಪಮಾನ (ಹೆಚ್ಚುತ್ತಿರುವ ಉಷ್ಣತೆಯು ವಿಘಟನೆಯನ್ನು ಉತ್ತೇಜಿಸುತ್ತದೆ), ಮತ್ತು ದ್ರಾವಕದ ಸ್ವರೂಪ (ಅಯಾನೀಕರಣವು ಮಾತ್ರ ಸಂಭವಿಸುತ್ತದೆ. ಧ್ರುವೀಯ ದ್ರಾವಕದಲ್ಲಿ, ನಿರ್ದಿಷ್ಟವಾಗಿ, ನೀರು).
ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳು ವಿದ್ಯುತ್ ಪ್ರವಾಹದ ಅಂಗೀಕಾರವನ್ನು ಅನುಮತಿಸುವ ಅಯಾನುಗಳ ಹೆಚ್ಚಿನ ಸಾಂದ್ರತೆಯನ್ನು ಹೊಂದಿರುವ ಪರಿಹಾರಗಳಾಗಿವೆ. ನಿಯಮದಂತೆ, ಇವುಗಳು ಲವಣಗಳು, ಆಮ್ಲಗಳು ಮತ್ತು ಕ್ಷಾರಗಳ ಜಲೀಯ ದ್ರಾವಣಗಳಾಗಿವೆ.
ಮಾನವ ಮತ್ತು ಪ್ರಾಣಿಗಳ ದೇಹದಲ್ಲಿ, ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳು ಪ್ರಮುಖ ಪಾತ್ರವನ್ನು ವಹಿಸುತ್ತವೆ: ಉದಾಹರಣೆಗೆ, ಕಬ್ಬಿಣದ ಅಯಾನುಗಳೊಂದಿಗೆ ರಕ್ತ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳು ಅಂಗಾಂಶಗಳಿಗೆ ಆಮ್ಲಜನಕವನ್ನು ಸಾಗಿಸುತ್ತವೆ; ಪೊಟ್ಯಾಸಿಯಮ್ ಮತ್ತು ಸೋಡಿಯಂ ಅಯಾನುಗಳೊಂದಿಗೆ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳು ದೇಹದ ನೀರು-ಉಪ್ಪು ಸಮತೋಲನ, ಕರುಳು ಮತ್ತು ಹೃದಯದ ಕಾರ್ಯವನ್ನು ನಿಯಂತ್ರಿಸುತ್ತದೆ.
ಗುಣಲಕ್ಷಣಗಳು
ಶುದ್ಧ ನೀರು, ಜಲರಹಿತ ಲವಣಗಳು, ಆಮ್ಲಗಳು ಮತ್ತು ಕ್ಷಾರಗಳು ಪ್ರವಾಹವನ್ನು ನಡೆಸುವುದಿಲ್ಲ. ದ್ರಾವಣಗಳಲ್ಲಿ, ವಸ್ತುಗಳು ಅಯಾನುಗಳಾಗಿ ವಿಭಜನೆಯಾಗುತ್ತವೆ ಮತ್ತು ಪ್ರವಾಹವನ್ನು ನಡೆಸುತ್ತವೆ. ಇದಕ್ಕಾಗಿಯೇ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳನ್ನು ಎರಡನೇ ಕ್ರಮಾಂಕದ ವಾಹಕಗಳು ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ (ಲೋಹಗಳಿಗೆ ವಿರುದ್ಧವಾಗಿ). ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳು ಕರಗುತ್ತವೆ ಮತ್ತು ಕೆಲವು ಹರಳುಗಳಾಗಿರಬಹುದು, ನಿರ್ದಿಷ್ಟವಾಗಿ ಜಿರ್ಕೋನಿಯಮ್ ಡೈಆಕ್ಸೈಡ್ ಮತ್ತು ಸಿಲ್ವರ್ ಅಯೋಡೈಡ್.
ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳ ಮುಖ್ಯ ಗುಣವೆಂದರೆ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯದ ವಿಘಟನೆಯ ಸಾಮರ್ಥ್ಯ, ಅಂದರೆ, ನೀರಿನ ಅಣುಗಳೊಂದಿಗೆ (ಅಥವಾ ಇತರ ದ್ರಾವಕಗಳು) ಚಾರ್ಜ್ಡ್ ಅಯಾನುಗಳಾಗಿ ಸಂವಹನ ಮಾಡುವಾಗ ಅಣುಗಳ ವಿಘಟನೆ.
ದ್ರಾವಣದಲ್ಲಿ ರೂಪುಗೊಂಡ ಅಯಾನುಗಳ ಪ್ರಕಾರವನ್ನು ಆಧರಿಸಿ, ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯವನ್ನು ಕ್ಷಾರೀಯ (ವಿದ್ಯುತ್ ವಾಹಕತೆಯು ಲೋಹದ ಅಯಾನುಗಳು ಮತ್ತು OH-), ಲವಣಯುಕ್ತ ಮತ್ತು ಆಮ್ಲೀಯ (H+ ಅಯಾನುಗಳು ಮತ್ತು ಆಸಿಡ್ ಬೇಸ್ ಶೇಷಗಳೊಂದಿಗೆ) ಎಂದು ಪ್ರತ್ಯೇಕಿಸಲಾಗಿದೆ.
ವಿಘಟನೆಯ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯದ ಸಾಮರ್ಥ್ಯವನ್ನು ಪರಿಮಾಣಾತ್ಮಕವಾಗಿ ನಿರೂಪಿಸಲು, "ಡಿಗ್ರಿ ಆಫ್ ಡಿಸೋಸಿಯೇಶನ್" ನಿಯತಾಂಕವನ್ನು ಪರಿಚಯಿಸಲಾಯಿತು. ಈ ಮೌಲ್ಯವು ಕೊಳೆತಕ್ಕೆ ಒಳಗಾದ ಅಣುಗಳ ಶೇಕಡಾವಾರು ಪ್ರಮಾಣವನ್ನು ಪ್ರತಿಬಿಂಬಿಸುತ್ತದೆ. ಇದು ಅವಲಂಬಿಸಿರುತ್ತದೆ:
ವಸ್ತುವೇ;
ದ್ರಾವಕ;
ವಸ್ತುವಿನ ಸಾಂದ್ರತೆ;
ತಾಪಮಾನ.
ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳನ್ನು ಬಲವಾದ ಮತ್ತು ದುರ್ಬಲವಾಗಿ ವಿಂಗಡಿಸಲಾಗಿದೆ. ಕಾರಕವು ಉತ್ತಮವಾಗಿ ಕರಗುತ್ತದೆ (ಅಯಾನುಗಳಾಗಿ ಒಡೆಯುತ್ತದೆ), ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯವು ಬಲವಾಗಿರುತ್ತದೆ, ಅದು ಉತ್ತಮವಾದ ಪ್ರವಾಹವನ್ನು ನಡೆಸುತ್ತದೆ. ಬಲವಾದ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳಲ್ಲಿ ಕ್ಷಾರಗಳು, ಬಲವಾದ ಆಮ್ಲಗಳು ಮತ್ತು ಕರಗುವ ಲವಣಗಳು ಸೇರಿವೆ.
ಬ್ಯಾಟರಿಗಳಲ್ಲಿ ಬಳಸಲಾಗುವ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳಿಗೆ, ಸಾಂದ್ರತೆಯಂತಹ ನಿಯತಾಂಕವು ಬಹಳ ಮುಖ್ಯವಾಗಿದೆ. ಬ್ಯಾಟರಿಯ ಕಾರ್ಯಾಚರಣೆಯ ಪರಿಸ್ಥಿತಿಗಳು, ಅದರ ಸಾಮರ್ಥ್ಯ ಮತ್ತು ಸೇವಾ ಜೀವನವು ಅದರ ಮೇಲೆ ಅವಲಂಬಿತವಾಗಿರುತ್ತದೆ. ಹೈಡ್ರೋಮೀಟರ್ ಬಳಸಿ ಸಾಂದ್ರತೆಯನ್ನು ನಿರ್ಧರಿಸಲಾಗುತ್ತದೆ.
ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳೊಂದಿಗೆ ಕೆಲಸ ಮಾಡುವಾಗ ಮುನ್ನೆಚ್ಚರಿಕೆಗಳು
ಅತ್ಯಂತ ಜನಪ್ರಿಯ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳು ಕೇಂದ್ರೀಕೃತ ಸಲ್ಫ್ಯೂರಿಕ್ ಆಮ್ಲ ಮತ್ತು ಕ್ಷಾರದ ಪರಿಹಾರವಾಗಿದೆ - ಹೆಚ್ಚಾಗಿ ಪೊಟ್ಯಾಸಿಯಮ್, ಸೋಡಿಯಂ ಮತ್ತು ಲಿಥಿಯಂ ಹೈಡ್ರಾಕ್ಸೈಡ್ಗಳು. ಇವೆಲ್ಲವೂ ಚರ್ಮ ಮತ್ತು ಲೋಳೆಯ ಪೊರೆಗಳಿಗೆ ರಾಸಾಯನಿಕ ಸುಡುವಿಕೆಗೆ ಕಾರಣವಾಗುತ್ತವೆ ಮತ್ತು ಕಣ್ಣುಗಳಿಗೆ ಅತ್ಯಂತ ಅಪಾಯಕಾರಿ ಸುಡುವಿಕೆಗೆ ಕಾರಣವಾಗುತ್ತವೆ. ಅದಕ್ಕಾಗಿಯೇ ಅಂತಹ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳೊಂದಿಗಿನ ಎಲ್ಲಾ ಕೆಲಸಗಳನ್ನು ಪ್ರತ್ಯೇಕ, ಚೆನ್ನಾಗಿ ಗಾಳಿ ಇರುವ ಕೋಣೆಯಲ್ಲಿ, ರಕ್ಷಣಾ ಸಾಧನಗಳನ್ನು ಬಳಸಿ ಮಾಡಬೇಕು: ಬಟ್ಟೆ, ಮುಖವಾಡಗಳು, ಕನ್ನಡಕಗಳು, ರಬ್ಬರ್ ಕೈಗವಸುಗಳು.
ತಟಸ್ಥಗೊಳಿಸುವ ಏಜೆಂಟ್ಗಳ ಗುಂಪಿನೊಂದಿಗೆ ಪ್ರಥಮ ಚಿಕಿತ್ಸಾ ಕಿಟ್ ಮತ್ತು ಎಲೆಕ್ಟ್ರೋಲೈಟ್ಗಳೊಂದಿಗೆ ಕೆಲಸ ಮಾಡುವ ಕೋಣೆಯ ಬಳಿ ನೀರಿನ ಟ್ಯಾಪ್ ಅನ್ನು ಇಡಬೇಕು.
ಆಸಿಡ್ ಬರ್ನ್ಸ್ ಅನ್ನು ಸೋಡಾದ ದ್ರಾವಣದೊಂದಿಗೆ ತಟಸ್ಥಗೊಳಿಸಲಾಗುತ್ತದೆ (1 ಕಪ್ ನೀರಿಗೆ 1 ಟೀಸ್ಪೂನ್).
ಅಲ್ಕಾಲಿ ಬರ್ನ್ಸ್ ಅನ್ನು ಬೋರಿಕ್ ಆಮ್ಲದ ದ್ರಾವಣದೊಂದಿಗೆ ತಟಸ್ಥಗೊಳಿಸಲಾಗುತ್ತದೆ (1 ಕಪ್ ನೀರಿಗೆ 1 ಟೀಸ್ಪೂನ್).
ಕಣ್ಣುಗಳನ್ನು ತೊಳೆಯಲು, ತಟಸ್ಥಗೊಳಿಸುವ ಪರಿಹಾರಗಳು ಎರಡು ಬಾರಿ ದುರ್ಬಲವಾಗಿರಬೇಕು.
ಹಾನಿಗೊಳಗಾದ ಚರ್ಮದ ಪ್ರದೇಶಗಳನ್ನು ಮೊದಲು ನ್ಯೂಟ್ರಾಲೈಸರ್ನಿಂದ ತೊಳೆಯಲಾಗುತ್ತದೆ, ಮತ್ತು ನಂತರ ಸೋಪ್ ಮತ್ತು ನೀರಿನಿಂದ ತೊಳೆಯಲಾಗುತ್ತದೆ.
ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯವನ್ನು ಚೆಲ್ಲಿದರೆ, ಅದನ್ನು ಮರದ ಪುಡಿಯಿಂದ ಸಂಗ್ರಹಿಸಲಾಗುತ್ತದೆ, ನಂತರ ನ್ಯೂಟ್ರಾಲೈಸರ್ನೊಂದಿಗೆ ತೊಳೆದು ಒಣಗಿಸಿ ಒರೆಸಲಾಗುತ್ತದೆ.
ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯದೊಂದಿಗೆ ಕೆಲಸ ಮಾಡುವಾಗ, ನೀವು ಮಾಡಬೇಕು  ಎಲ್ಲಾ ಸುರಕ್ಷತೆ ಅವಶ್ಯಕತೆಗಳು. ಉದಾಹರಣೆಗೆ, ಆಮ್ಲವನ್ನು ನೀರಿನಲ್ಲಿ ಸುರಿಯಲಾಗುತ್ತದೆ (ಮತ್ತು ಪ್ರತಿಯಾಗಿ ಅಲ್ಲ!) ಕೈಯಾರೆ ಅಲ್ಲ, ಆದರೆ ಸಾಧನಗಳ ಸಹಾಯದಿಂದ. ಘನ ಕ್ಷಾರದ ತುಂಡುಗಳನ್ನು ನಿಮ್ಮ ಕೈಗಳಿಂದ ಅಲ್ಲ, ಆದರೆ ಇಕ್ಕುಳಗಳು ಅಥವಾ ಚಮಚಗಳೊಂದಿಗೆ ನೀರಿನಲ್ಲಿ ಇಳಿಸಲಾಗುತ್ತದೆ. ವಿವಿಧ ರೀತಿಯ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳೊಂದಿಗೆ ಬ್ಯಾಟರಿಗಳೊಂದಿಗೆ ಒಂದೇ ಕೋಣೆಯಲ್ಲಿ ನೀವು ಕೆಲಸ ಮಾಡಲು ಸಾಧ್ಯವಿಲ್ಲ, ಮತ್ತು ಅವುಗಳನ್ನು ಒಟ್ಟಿಗೆ ಸಂಗ್ರಹಿಸುವುದನ್ನು ಸಹ ನಿಷೇಧಿಸಲಾಗಿದೆ.
ಎಲ್ಲಾ ಸುರಕ್ಷತೆ ಅವಶ್ಯಕತೆಗಳು. ಉದಾಹರಣೆಗೆ, ಆಮ್ಲವನ್ನು ನೀರಿನಲ್ಲಿ ಸುರಿಯಲಾಗುತ್ತದೆ (ಮತ್ತು ಪ್ರತಿಯಾಗಿ ಅಲ್ಲ!) ಕೈಯಾರೆ ಅಲ್ಲ, ಆದರೆ ಸಾಧನಗಳ ಸಹಾಯದಿಂದ. ಘನ ಕ್ಷಾರದ ತುಂಡುಗಳನ್ನು ನಿಮ್ಮ ಕೈಗಳಿಂದ ಅಲ್ಲ, ಆದರೆ ಇಕ್ಕುಳಗಳು ಅಥವಾ ಚಮಚಗಳೊಂದಿಗೆ ನೀರಿನಲ್ಲಿ ಇಳಿಸಲಾಗುತ್ತದೆ. ವಿವಿಧ ರೀತಿಯ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳೊಂದಿಗೆ ಬ್ಯಾಟರಿಗಳೊಂದಿಗೆ ಒಂದೇ ಕೋಣೆಯಲ್ಲಿ ನೀವು ಕೆಲಸ ಮಾಡಲು ಸಾಧ್ಯವಿಲ್ಲ, ಮತ್ತು ಅವುಗಳನ್ನು ಒಟ್ಟಿಗೆ ಸಂಗ್ರಹಿಸುವುದನ್ನು ಸಹ ನಿಷೇಧಿಸಲಾಗಿದೆ.
ಕೆಲವು ಕೆಲಸಗಳಿಗೆ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯವನ್ನು "ಕುದಿಯುವ" ಅಗತ್ಯವಿರುತ್ತದೆ. ಇದು ಹೈಡ್ರೋಜನ್, ಸುಡುವ ಮತ್ತು ಸ್ಫೋಟಕ ಅನಿಲವನ್ನು ಬಿಡುಗಡೆ ಮಾಡುತ್ತದೆ. ಅಂತಹ ಆವರಣದಲ್ಲಿ, ಸ್ಫೋಟ-ನಿರೋಧಕ ವಿದ್ಯುತ್ ವೈರಿಂಗ್ ಮತ್ತು ವಿದ್ಯುತ್ ಉಪಕರಣಗಳನ್ನು ಬಳಸಬೇಕು, ಧೂಮಪಾನ ಮತ್ತು ತೆರೆದ ಜ್ವಾಲೆಯೊಂದಿಗೆ ಯಾವುದೇ ಕೆಲಸವನ್ನು ನಿಷೇಧಿಸಲಾಗಿದೆ.
ಪ್ಲಾಸ್ಟಿಕ್ ಪಾತ್ರೆಗಳಲ್ಲಿ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳನ್ನು ಸಂಗ್ರಹಿಸಿ. ಗಾಜು, ಸೆರಾಮಿಕ್, ಪಿಂಗಾಣಿ ಭಕ್ಷ್ಯಗಳು ಮತ್ತು ಉಪಕರಣಗಳು ಕೆಲಸಕ್ಕೆ ಸೂಕ್ತವಾಗಿವೆ.
ಮುಂದಿನ ಲೇಖನದಲ್ಲಿ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯದ ವಿಧಗಳು ಮತ್ತು ಉಪಯೋಗಗಳ ಬಗ್ಗೆ ನಾವು ನಿಮಗೆ ಹೆಚ್ಚು ಹೇಳುತ್ತೇವೆ.
ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳನ್ನು ರಾಸಾಯನಿಕ ಪದಾರ್ಥಗಳಾಗಿ ಪ್ರಾಚೀನ ಕಾಲದಿಂದಲೂ ಕರೆಯಲಾಗುತ್ತದೆ. ಆದಾಗ್ಯೂ, ಅವರು ತುಲನಾತ್ಮಕವಾಗಿ ಇತ್ತೀಚೆಗೆ ತಮ್ಮ ಅಪ್ಲಿಕೇಶನ್ನ ಹೆಚ್ಚಿನ ಪ್ರದೇಶಗಳನ್ನು ವಶಪಡಿಸಿಕೊಂಡಿದ್ದಾರೆ. ಈ ಪದಾರ್ಥಗಳನ್ನು ಬಳಸುವುದಕ್ಕಾಗಿ ನಾವು ಉದ್ಯಮದ ಹೆಚ್ಚಿನ ಆದ್ಯತೆಯ ಕ್ಷೇತ್ರಗಳನ್ನು ಚರ್ಚಿಸುತ್ತೇವೆ ಮತ್ತು ಎರಡನೆಯದು ಯಾವುದು ಮತ್ತು ಅವು ಪರಸ್ಪರ ಹೇಗೆ ಭಿನ್ನವಾಗಿವೆ ಎಂಬುದನ್ನು ಲೆಕ್ಕಾಚಾರ ಮಾಡುತ್ತೇವೆ. ಆದರೆ ಇತಿಹಾಸದ ವಿಹಾರದೊಂದಿಗೆ ಪ್ರಾರಂಭಿಸೋಣ.
ಕಥೆ
ಪ್ರಾಚೀನ ಜಗತ್ತಿನಲ್ಲಿ ಪತ್ತೆಯಾದ ಲವಣಗಳು ಮತ್ತು ಆಮ್ಲಗಳು ಅತ್ಯಂತ ಹಳೆಯ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳಾಗಿವೆ. ಆದಾಗ್ಯೂ, ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳ ರಚನೆ ಮತ್ತು ಗುಣಲಕ್ಷಣಗಳ ಬಗ್ಗೆ ಕಲ್ಪನೆಗಳು ಕಾಲಾನಂತರದಲ್ಲಿ ವಿಕಸನಗೊಂಡಿವೆ. ಈ ಪ್ರಕ್ರಿಯೆಗಳ ಸಿದ್ಧಾಂತಗಳು 1880 ರ ದಶಕದಿಂದ ವಿಕಸನಗೊಂಡಿವೆ, ಎಲೆಕ್ಟ್ರೋಲೈಟ್ಗಳ ಗುಣಲಕ್ಷಣಗಳ ಸಿದ್ಧಾಂತಗಳಿಗೆ ಸಂಬಂಧಿಸಿದಂತೆ ಹಲವಾರು ಆವಿಷ್ಕಾರಗಳನ್ನು ಮಾಡಲಾಯಿತು. ನೀರಿನೊಂದಿಗೆ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳ ಪರಸ್ಪರ ಕ್ರಿಯೆಯ ಕಾರ್ಯವಿಧಾನಗಳನ್ನು ವಿವರಿಸುವ ಸಿದ್ಧಾಂತಗಳಲ್ಲಿ ಹಲವಾರು ಗುಣಾತ್ಮಕ ಚಿಮ್ಮುವಿಕೆಗಳನ್ನು ಗಮನಿಸಲಾಗಿದೆ (ಎಲ್ಲಾ ನಂತರ, ಪರಿಹಾರದಲ್ಲಿ ಮಾತ್ರ ಅವರು ಉದ್ಯಮದಲ್ಲಿ ಬಳಸಲಾಗುವ ಗುಣಲಕ್ಷಣಗಳನ್ನು ಪಡೆದುಕೊಳ್ಳುತ್ತಾರೆ).
ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳು ಮತ್ತು ಅವುಗಳ ಗುಣಲಕ್ಷಣಗಳ ಬಗ್ಗೆ ಕಲ್ಪನೆಗಳ ಅಭಿವೃದ್ಧಿಯ ಮೇಲೆ ಹೆಚ್ಚಿನ ಪ್ರಭಾವ ಬೀರಿದ ಹಲವಾರು ಸಿದ್ಧಾಂತಗಳನ್ನು ಈಗ ನಾವು ವಿವರವಾಗಿ ಪರಿಶೀಲಿಸುತ್ತೇವೆ. ಮತ್ತು ನಮ್ಮಲ್ಲಿ ಪ್ರತಿಯೊಬ್ಬರೂ ಶಾಲೆಯಲ್ಲಿ ಹಾದುಹೋದ ಅತ್ಯಂತ ಸಾಮಾನ್ಯ ಮತ್ತು ಸರಳವಾದ ಸಿದ್ಧಾಂತದೊಂದಿಗೆ ಪ್ರಾರಂಭಿಸೋಣ.
ಎಲೆಕ್ಟ್ರೋಲೈಟಿಕ್ ಡಿಸೋಸಿಯೇಶನ್ನ ಅರ್ಹೆನಿಯಸ್ ಸಿದ್ಧಾಂತ
1887 ರಲ್ಲಿ, ಸ್ವೀಡಿಷ್ ರಸಾಯನಶಾಸ್ತ್ರಜ್ಞ ಮತ್ತು ವಿಲ್ಹೆಲ್ಮ್ ಓಸ್ಟ್ವಾಲ್ಡ್ ಎಲೆಕ್ಟ್ರೋಲೈಟಿಕ್ ಡಿಸೋಸಿಯೇಶನ್ ಸಿದ್ಧಾಂತವನ್ನು ರಚಿಸಿದರು. ಆದಾಗ್ಯೂ, ಇಲ್ಲಿಯೂ ಅದು ಅಷ್ಟು ಸುಲಭವಲ್ಲ. ಅರ್ಹೆನಿಯಸ್ ಸ್ವತಃ ಪರಿಹಾರಗಳ ಭೌತಿಕ ಸಿದ್ಧಾಂತ ಎಂದು ಕರೆಯಲ್ಪಡುವ ಪ್ರತಿಪಾದಕರಾಗಿದ್ದರು, ಇದು ನೀರಿನೊಂದಿಗೆ ವಸ್ತುವಿನ ಘಟಕಗಳ ಪರಸ್ಪರ ಕ್ರಿಯೆಯನ್ನು ಗಣನೆಗೆ ತೆಗೆದುಕೊಳ್ಳಲಿಲ್ಲ ಮತ್ತು ಮುಕ್ತ ಚಾರ್ಜ್ಡ್ ಕಣಗಳು (ಅಯಾನುಗಳು) ದ್ರಾವಣದಲ್ಲಿ ಅಸ್ತಿತ್ವದಲ್ಲಿವೆ ಎಂದು ವಾದಿಸಿದರು. ಮೂಲಕ, ಇಂದು ಶಾಲೆಯಲ್ಲಿ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯ ವಿಘಟನೆಯನ್ನು ಪರಿಗಣಿಸಲಾಗುತ್ತದೆ ಎಂದು ಈ ಸ್ಥಾನದಿಂದ.
ಈ ಸಿದ್ಧಾಂತವು ಏನನ್ನು ಒದಗಿಸುತ್ತದೆ ಮತ್ತು ನೀರಿನೊಂದಿಗೆ ವಸ್ತುಗಳ ಪರಸ್ಪರ ಕ್ರಿಯೆಯ ಕಾರ್ಯವಿಧಾನವನ್ನು ನಮಗೆ ಹೇಗೆ ವಿವರಿಸುತ್ತದೆ ಎಂಬುದರ ಕುರಿತು ಮಾತನಾಡೋಣ. ಇತರರಂತೆ, ಅವಳು ಬಳಸುವ ಹಲವಾರು ಪೋಸ್ಟುಲೇಟ್ಗಳನ್ನು ಹೊಂದಿದ್ದಾಳೆ:
1. ನೀರಿನೊಂದಿಗೆ ಸಂವಹನ ಮಾಡುವಾಗ, ವಸ್ತುವು ಅಯಾನುಗಳಾಗಿ ವಿಭಜಿಸುತ್ತದೆ (ಧನಾತ್ಮಕ - ಕ್ಯಾಷನ್ ಮತ್ತು ಋಣಾತ್ಮಕ - ಅಯಾನ್). ಈ ಕಣಗಳು ಜಲಸಂಚಯನಕ್ಕೆ ಒಳಗಾಗುತ್ತವೆ: ಅವು ನೀರಿನ ಅಣುಗಳನ್ನು ಆಕರ್ಷಿಸುತ್ತವೆ, ಇದು ಒಂದು ಬದಿಯಲ್ಲಿ ಧನಾತ್ಮಕವಾಗಿ ಮತ್ತು ಇನ್ನೊಂದು ಬದಿಯಲ್ಲಿ ಋಣಾತ್ಮಕವಾಗಿ ಚಾರ್ಜ್ ಆಗುತ್ತದೆ (ದ್ವಿಧ್ರುವಿಯನ್ನು ರೂಪಿಸುತ್ತದೆ), ಇದರ ಪರಿಣಾಮವಾಗಿ ಅವು ಆಕ್ವಾ ಸಂಕೀರ್ಣಗಳಾಗಿ (ಸಾಲ್ವೇಟ್ಸ್) ರೂಪುಗೊಳ್ಳುತ್ತವೆ.
2. ವಿಘಟನೆಯ ಪ್ರಕ್ರಿಯೆಯು ಹಿಂತಿರುಗಿಸಬಲ್ಲದು - ಅಂದರೆ, ಒಂದು ವಸ್ತುವು ಅಯಾನುಗಳಾಗಿ ವಿಭಜನೆಯಾಗಿದ್ದರೆ, ಯಾವುದೇ ಅಂಶಗಳ ಪ್ರಭಾವದ ಅಡಿಯಲ್ಲಿ ಅದು ಮತ್ತೆ ಅದರ ಮೂಲ ರೂಪಕ್ಕೆ ಬದಲಾಗಬಹುದು.
3. ನೀವು ವಿದ್ಯುದ್ವಾರಗಳನ್ನು ಪರಿಹಾರಕ್ಕೆ ಸಂಪರ್ಕಿಸಿದರೆ ಮತ್ತು ಪ್ರಸ್ತುತವನ್ನು ಆನ್ ಮಾಡಿದರೆ, ಕ್ಯಾಟಯಾನುಗಳು ಋಣಾತ್ಮಕ ವಿದ್ಯುದ್ವಾರಕ್ಕೆ ಚಲಿಸಲು ಪ್ರಾರಂಭಿಸುತ್ತವೆ - ಕ್ಯಾಥೋಡ್, ಮತ್ತು ಅಯಾನುಗಳು ಧನಾತ್ಮಕ ಆವೇಶದ ಒಂದಕ್ಕೆ - ಆನೋಡ್. ಅದಕ್ಕಾಗಿಯೇ ನೀರಿನಲ್ಲಿ ಹೆಚ್ಚು ಕರಗುವ ವಸ್ತುಗಳು ನೀರಿಗಿಂತ ಉತ್ತಮವಾಗಿ ವಿದ್ಯುತ್ ಪ್ರವಾಹವನ್ನು ನಡೆಸುತ್ತವೆ. ಅದೇ ಕಾರಣಕ್ಕಾಗಿ ಅವುಗಳನ್ನು ಎಲೆಕ್ಟ್ರೋಲೈಟ್ಸ್ ಎಂದು ಕರೆಯಲಾಯಿತು.
4. ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯವು ವಿಸರ್ಜನೆಗೆ ಒಳಗಾದ ವಸ್ತುವಿನ ಶೇಕಡಾವಾರು ಪ್ರಮಾಣವನ್ನು ನಿರೂಪಿಸುತ್ತದೆ. ಈ ಸೂಚಕವು ದ್ರಾವಕದ ಗುಣಲಕ್ಷಣಗಳನ್ನು ಮತ್ತು ಕರಗಿದ ವಸ್ತುವಿನ ಮೇಲೆ ಅವಲಂಬಿತವಾಗಿರುತ್ತದೆ, ನಂತರದ ಸಾಂದ್ರತೆಯ ಮೇಲೆ ಮತ್ತು ಬಾಹ್ಯ ತಾಪಮಾನದ ಮೇಲೆ.
ಇಲ್ಲಿ, ವಾಸ್ತವವಾಗಿ, ಈ ಸರಳ ಸಿದ್ಧಾಂತದ ಎಲ್ಲಾ ಮುಖ್ಯ ಪೋಸ್ಟುಲೇಟ್ಗಳು. ಎಲೆಕ್ಟ್ರೋಲೈಟ್ ದ್ರಾವಣದಲ್ಲಿ ಏನಾಗುತ್ತದೆ ಎಂಬುದನ್ನು ವಿವರಿಸಲು ನಾವು ಈ ಲೇಖನದಲ್ಲಿ ಅವುಗಳನ್ನು ಬಳಸುತ್ತೇವೆ. ಈ ಸಂಪರ್ಕಗಳ ಉದಾಹರಣೆಗಳನ್ನು ನಾವು ಸ್ವಲ್ಪ ಸಮಯದ ನಂತರ ನೋಡುತ್ತೇವೆ, ಆದರೆ ಈಗ ಇನ್ನೊಂದು ಸಿದ್ಧಾಂತವನ್ನು ನೋಡೋಣ.

ಆಮ್ಲಗಳು ಮತ್ತು ಕ್ಷಾರಗಳ ಲೆವಿಸ್ ಸಿದ್ಧಾಂತ
ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯ ವಿಘಟನೆಯ ಸಿದ್ಧಾಂತದ ಪ್ರಕಾರ, ಆಮ್ಲವು ಹೈಡ್ರೋಜನ್ ಕ್ಯಾಷನ್ ಇರುವ ದ್ರಾವಣದಲ್ಲಿ ಒಂದು ವಸ್ತುವಾಗಿದೆ, ಮತ್ತು ಬೇಸ್ ಎಂಬುದು ಹೈಡ್ರಾಕ್ಸೈಡ್ ಅಯಾನ್ ಆಗಿ ದ್ರಾವಣದಲ್ಲಿ ವಿಭಜನೆಯಾಗುವ ಸಂಯುಕ್ತವಾಗಿದೆ. ಪ್ರಸಿದ್ಧ ರಸಾಯನಶಾಸ್ತ್ರಜ್ಞ ಗಿಲ್ಬರ್ಟ್ ಲೂಯಿಸ್ ಅವರ ಹೆಸರಿನ ಮತ್ತೊಂದು ಸಿದ್ಧಾಂತವಿದೆ. ಇದು ಆಮ್ಲ ಮತ್ತು ಬೇಸ್ ಪರಿಕಲ್ಪನೆಯನ್ನು ಸ್ವಲ್ಪಮಟ್ಟಿಗೆ ವಿಸ್ತರಿಸಲು ನಮಗೆ ಅನುಮತಿಸುತ್ತದೆ. ಲೆವಿಸ್ ಸಿದ್ಧಾಂತದ ಪ್ರಕಾರ, ಆಮ್ಲಗಳು ಒಂದು ವಸ್ತುವಿನ ಅಣುಗಳಾಗಿವೆ, ಅದು ಉಚಿತ ಎಲೆಕ್ಟ್ರಾನ್ ಕಕ್ಷೆಗಳನ್ನು ಹೊಂದಿದೆ ಮತ್ತು ಇನ್ನೊಂದು ಅಣುವಿನಿಂದ ಎಲೆಕ್ಟ್ರಾನ್ ಅನ್ನು ಸ್ವೀಕರಿಸುವ ಸಾಮರ್ಥ್ಯವನ್ನು ಹೊಂದಿದೆ. ಆಮ್ಲದ "ಬಳಕೆ" ಗೆ ತಮ್ಮ ಒಂದು ಅಥವಾ ಹೆಚ್ಚಿನ ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ದಾನ ಮಾಡಲು ಸಮರ್ಥವಾಗಿರುವ ಕಣಗಳು ಬೇಸ್ಗಳಾಗಿರುತ್ತವೆ ಎಂದು ಊಹಿಸುವುದು ಸುಲಭ. ಇಲ್ಲಿ ಬಹಳ ಆಸಕ್ತಿದಾಯಕ ಸಂಗತಿಯೆಂದರೆ, ಎಲೆಕ್ಟ್ರೋಲೈಟ್ ಮಾತ್ರವಲ್ಲ, ನೀರಿನಲ್ಲಿ ಕರಗದ ಯಾವುದೇ ವಸ್ತುವೂ ಸಹ ಆಮ್ಲ ಅಥವಾ ಬೇಸ್ ಆಗಿರಬಹುದು.

ಬ್ರೆಂಡ್ಸ್ಟೆಡ್-ಲೋರಿ ಪ್ರೊಟೊಲಿಟಿಕ್ ಸಿದ್ಧಾಂತ
1923 ರಲ್ಲಿ, ಪರಸ್ಪರ ಸ್ವತಂತ್ರವಾಗಿ, ಇಬ್ಬರು ವಿಜ್ಞಾನಿಗಳು - ಜೆ. ಬ್ರಾನ್ಸ್ಟೆಡ್ ಮತ್ತು ಟಿ. ಲೋರಿ - ರಾಸಾಯನಿಕ ಪ್ರಕ್ರಿಯೆಗಳನ್ನು ವಿವರಿಸಲು ವಿಜ್ಞಾನಿಗಳು ಈಗ ಸಕ್ರಿಯವಾಗಿ ಬಳಸುತ್ತಿರುವ ಸಿದ್ಧಾಂತವನ್ನು ಪ್ರಸ್ತಾಪಿಸಿದರು. ಈ ಸಿದ್ಧಾಂತದ ಸಾರವೆಂದರೆ ವಿಘಟನೆಯ ಅರ್ಥವು ಪ್ರೋಟಾನ್ ಅನ್ನು ಆಮ್ಲದಿಂದ ಬೇಸ್ಗೆ ವರ್ಗಾಯಿಸಲು ಬರುತ್ತದೆ. ಹೀಗಾಗಿ, ಎರಡನೆಯದನ್ನು ಇಲ್ಲಿ ಪ್ರೋಟಾನ್ ಸ್ವೀಕಾರಕ ಎಂದು ಅರ್ಥೈಸಿಕೊಳ್ಳಲಾಗಿದೆ. ಆಗ ಆಸಿಡ್ ಅವರ ದಾನಿ. ಈ ಸಿದ್ಧಾಂತವು ಆಮ್ಲಗಳು ಮತ್ತು ಬೇಸ್ಗಳ ಗುಣಲಕ್ಷಣಗಳನ್ನು ಪ್ರದರ್ಶಿಸುವ ವಸ್ತುಗಳ ಅಸ್ತಿತ್ವವನ್ನು ಚೆನ್ನಾಗಿ ವಿವರಿಸುತ್ತದೆ. ಅಂತಹ ಸಂಯುಕ್ತಗಳನ್ನು ಆಂಫೋಟೆರಿಕ್ ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ. ಬ್ರಾನ್ಸ್ಟೆಡ್-ಲೋರಿ ಸಿದ್ಧಾಂತದಲ್ಲಿ, ಆಂಫೋಲೈಟ್ಸ್ ಎಂಬ ಪದವನ್ನು ಸಹ ಬಳಸಲಾಗುತ್ತದೆ, ಆದರೆ ಆಮ್ಲಗಳು ಅಥವಾ ಬೇಸ್ಗಳನ್ನು ಸಾಮಾನ್ಯವಾಗಿ ಪ್ರೋಟೋಲೈಟ್ಗಳು ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ.
ನಾವು ಲೇಖನದ ಮುಂದಿನ ಭಾಗಕ್ಕೆ ಬರುತ್ತೇವೆ. ಪ್ರಬಲ ಮತ್ತು ದುರ್ಬಲ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳು ಪರಸ್ಪರ ಹೇಗೆ ಭಿನ್ನವಾಗಿರುತ್ತವೆ ಮತ್ತು ಅವುಗಳ ಗುಣಲಕ್ಷಣಗಳ ಮೇಲೆ ಬಾಹ್ಯ ಅಂಶಗಳ ಪ್ರಭಾವವನ್ನು ಚರ್ಚಿಸಲು ಇಲ್ಲಿ ನಾವು ನಿಮಗೆ ಹೇಳುತ್ತೇವೆ. ತದನಂತರ ನಾವು ಅವರ ಪ್ರಾಯೋಗಿಕ ಅಪ್ಲಿಕೇಶನ್ ಅನ್ನು ವಿವರಿಸಲು ಪ್ರಾರಂಭಿಸುತ್ತೇವೆ.
ಬಲವಾದ ಮತ್ತು ದುರ್ಬಲ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳು
ಪ್ರತಿಯೊಂದು ವಸ್ತುವು ಪ್ರತ್ಯೇಕವಾಗಿ ನೀರಿನೊಂದಿಗೆ ಸಂವಹನ ನಡೆಸುತ್ತದೆ. ಕೆಲವು ಅದರಲ್ಲಿ ಚೆನ್ನಾಗಿ ಕರಗುತ್ತವೆ (ಉದಾಹರಣೆಗೆ, ಟೇಬಲ್ ಉಪ್ಪು), ಇತರರು ಎಲ್ಲವನ್ನೂ ಕರಗಿಸುವುದಿಲ್ಲ (ಉದಾಹರಣೆಗೆ, ಸೀಮೆಸುಣ್ಣ). ಹೀಗಾಗಿ, ಎಲ್ಲಾ ಪದಾರ್ಥಗಳನ್ನು ಬಲವಾದ ಮತ್ತು ದುರ್ಬಲ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳಾಗಿ ವಿಂಗಡಿಸಲಾಗಿದೆ. ಎರಡನೆಯದು ನೀರಿನೊಂದಿಗೆ ಕಳಪೆಯಾಗಿ ಸಂವಹನ ನಡೆಸುವ ಮತ್ತು ದ್ರಾವಣದ ಕೆಳಭಾಗದಲ್ಲಿ ನೆಲೆಗೊಳ್ಳುವ ವಸ್ತುಗಳು. ಇದರರ್ಥ ಅವುಗಳು ಅತ್ಯಂತ ಕಡಿಮೆ ಮಟ್ಟದ ವಿಘಟನೆ ಮತ್ತು ಹೆಚ್ಚಿನ ಬಂಧದ ಶಕ್ತಿಯನ್ನು ಹೊಂದಿರುತ್ತವೆ, ಇದು ಸಾಮಾನ್ಯ ಪರಿಸ್ಥಿತಿಗಳಲ್ಲಿ ಅಣುವು ಅದರ ಘಟಕ ಅಯಾನುಗಳಾಗಿ ವಿಭಜನೆಯಾಗಲು ಅನುಮತಿಸುವುದಿಲ್ಲ. ದುರ್ಬಲ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳ ವಿಘಟನೆಯು ಬಹಳ ನಿಧಾನವಾಗಿ ಅಥವಾ ಹೆಚ್ಚುತ್ತಿರುವ ತಾಪಮಾನ ಮತ್ತು ದ್ರಾವಣದಲ್ಲಿ ಈ ವಸ್ತುವಿನ ಸಾಂದ್ರತೆಯೊಂದಿಗೆ ಸಂಭವಿಸುತ್ತದೆ.
ಬಲವಾದ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳ ಬಗ್ಗೆ ಮಾತನಾಡೋಣ. ಇವುಗಳಲ್ಲಿ ಎಲ್ಲಾ ಕರಗುವ ಲವಣಗಳು, ಹಾಗೆಯೇ ಬಲವಾದ ಆಮ್ಲಗಳು ಮತ್ತು ಕ್ಷಾರಗಳು ಸೇರಿವೆ. ಅವು ಸುಲಭವಾಗಿ ಅಯಾನುಗಳಾಗಿ ವಿಭಜನೆಯಾಗುತ್ತವೆ ಮತ್ತು ಮಳೆಯಾಗಿ ಸಂಗ್ರಹಿಸಲು ತುಂಬಾ ಕಷ್ಟ. ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳಲ್ಲಿ ಪ್ರಸ್ತುತ, ಮೂಲಕ, ದ್ರಾವಣದಲ್ಲಿ ಒಳಗೊಂಡಿರುವ ಅಯಾನುಗಳಿಗೆ ನಿಖರವಾಗಿ ಧನ್ಯವಾದಗಳು ಕೈಗೊಳ್ಳಲಾಗುತ್ತದೆ. ಆದ್ದರಿಂದ, ಬಲವಾದ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳು ಪ್ರಸ್ತುತವನ್ನು ಉತ್ತಮವಾಗಿ ನಡೆಸುತ್ತವೆ. ನಂತರದ ಉದಾಹರಣೆಗಳು: ಬಲವಾದ ಆಮ್ಲಗಳು, ಕ್ಷಾರಗಳು, ಕರಗುವ ಲವಣಗಳು.
ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳ ವರ್ತನೆಯ ಮೇಲೆ ಪ್ರಭಾವ ಬೀರುವ ಅಂಶಗಳು
ಬಾಹ್ಯ ಪರಿಸರದಲ್ಲಿನ ಬದಲಾವಣೆಗಳು ಹೇಗೆ ಪರಿಣಾಮ ಬೀರುತ್ತವೆ ಎಂಬುದನ್ನು ಈಗ ಲೆಕ್ಕಾಚಾರ ಮಾಡೋಣ ಏಕಾಗ್ರತೆಯು ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯದ ವಿಘಟನೆಯ ಮಟ್ಟವನ್ನು ನೇರವಾಗಿ ಪರಿಣಾಮ ಬೀರುತ್ತದೆ. ಇದಲ್ಲದೆ, ಈ ಸಂಬಂಧವನ್ನು ಗಣಿತದ ಮೂಲಕ ವ್ಯಕ್ತಪಡಿಸಬಹುದು. ಈ ಸಂಬಂಧವನ್ನು ವಿವರಿಸುವ ಕಾನೂನನ್ನು ಓಸ್ಟ್ವಾಲ್ಡ್ನ ದುರ್ಬಲಗೊಳಿಸುವ ಕಾನೂನು ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ ಮತ್ತು ಈ ಕೆಳಗಿನಂತೆ ಬರೆಯಲಾಗಿದೆ: a = (K / c) 1/2. ಇಲ್ಲಿ a ಎಂಬುದು ವಿಘಟನೆಯ ಮಟ್ಟವಾಗಿದೆ (ಭಿನ್ನರಾಶಿಗಳಲ್ಲಿ ತೆಗೆದುಕೊಳ್ಳಲಾಗಿದೆ), K ಎಂಬುದು ವಿಘಟನೆಯ ಸ್ಥಿರವಾಗಿರುತ್ತದೆ, ಪ್ರತಿ ವಸ್ತುವಿಗೂ ವಿಭಿನ್ನವಾಗಿರುತ್ತದೆ ಮತ್ತು c ಎಂಬುದು ದ್ರಾವಣದಲ್ಲಿನ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯದ ಸಾಂದ್ರತೆಯಾಗಿದೆ. ಈ ಸೂತ್ರವನ್ನು ಬಳಸಿಕೊಂಡು, ನೀವು ವಸ್ತುವಿನ ಬಗ್ಗೆ ಮತ್ತು ದ್ರಾವಣದಲ್ಲಿ ಅದರ ನಡವಳಿಕೆಯ ಬಗ್ಗೆ ಬಹಳಷ್ಟು ಕಲಿಯಬಹುದು.
ಆದರೆ ನಾವು ವಿಷಯದಿಂದ ವಿಮುಖರಾಗಿದ್ದೇವೆ. ಏಕಾಗ್ರತೆಯ ಜೊತೆಗೆ, ವಿಘಟನೆಯ ಮಟ್ಟವು ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯದ ಉಷ್ಣತೆಯಿಂದ ಕೂಡ ಪ್ರಭಾವಿತವಾಗಿರುತ್ತದೆ. ಹೆಚ್ಚಿನ ವಸ್ತುಗಳಿಗೆ, ಅದನ್ನು ಹೆಚ್ಚಿಸುವುದರಿಂದ ಕರಗುವಿಕೆ ಮತ್ತು ರಾಸಾಯನಿಕ ಚಟುವಟಿಕೆಯನ್ನು ಹೆಚ್ಚಿಸುತ್ತದೆ. ಎತ್ತರದ ತಾಪಮಾನದಲ್ಲಿ ಮಾತ್ರ ಕೆಲವು ಪ್ರತಿಕ್ರಿಯೆಗಳ ಸಂಭವವನ್ನು ಇದು ನಿಖರವಾಗಿ ವಿವರಿಸುತ್ತದೆ. ಸಾಮಾನ್ಯ ಪರಿಸ್ಥಿತಿಗಳಲ್ಲಿ, ಅವರು ನಿಧಾನವಾಗಿ ಅಥವಾ ಎರಡೂ ದಿಕ್ಕುಗಳಲ್ಲಿ ಹೋಗುತ್ತಾರೆ (ಈ ಪ್ರಕ್ರಿಯೆಯನ್ನು ರಿವರ್ಸಿಬಲ್ ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ).
ಎಲೆಕ್ಟ್ರೋಲೈಟ್ ದ್ರಾವಣದಂತಹ ವ್ಯವಸ್ಥೆಯ ವರ್ತನೆಯನ್ನು ನಿರ್ಧರಿಸುವ ಅಂಶಗಳನ್ನು ನಾವು ವಿಶ್ಲೇಷಿಸಿದ್ದೇವೆ. ಈಗ ಇವುಗಳ ಪ್ರಾಯೋಗಿಕ ಅನ್ವಯಕ್ಕೆ ಹೋಗೋಣ, ನಿಸ್ಸಂದೇಹವಾಗಿ, ಬಹಳ ಮುಖ್ಯವಾದ ರಾಸಾಯನಿಕಗಳು.

ಕೈಗಾರಿಕಾ ಬಳಕೆ
ಸಹಜವಾಗಿ, ಪ್ರತಿಯೊಬ್ಬರೂ ಬ್ಯಾಟರಿಗಳಿಗೆ ಸಂಬಂಧಿಸಿದಂತೆ "ಎಲೆಕ್ಟ್ರೋಲೈಟ್" ಎಂಬ ಪದವನ್ನು ಕೇಳಿದ್ದಾರೆ. ಕಾರು ಸೀಸ-ಆಮ್ಲ ಬ್ಯಾಟರಿಗಳನ್ನು ಬಳಸುತ್ತದೆ, ಎಲೆಕ್ಟ್ರೋಲೈಟ್ ಇದರಲ್ಲಿ 40% ಸಲ್ಫ್ಯೂರಿಕ್ ಆಮ್ಲ. ಈ ವಸ್ತುವು ಅಲ್ಲಿ ಏಕೆ ಬೇಕು ಎಂಬುದನ್ನು ಅರ್ಥಮಾಡಿಕೊಳ್ಳಲು, ಬ್ಯಾಟರಿಗಳ ಕಾರ್ಯಾಚರಣಾ ವೈಶಿಷ್ಟ್ಯಗಳನ್ನು ಅರ್ಥಮಾಡಿಕೊಳ್ಳುವುದು ಯೋಗ್ಯವಾಗಿದೆ.
ಆದ್ದರಿಂದ ಯಾವುದೇ ಬ್ಯಾಟರಿಯ ಕಾರ್ಯಾಚರಣೆಯ ತತ್ವ ಏನು? ಅವರು ಒಂದು ವಸ್ತುವನ್ನು ಇನ್ನೊಂದಕ್ಕೆ ಪರಿವರ್ತಿಸುವ ರಿವರ್ಸಿಬಲ್ ಪ್ರತಿಕ್ರಿಯೆಗೆ ಒಳಗಾಗುತ್ತಾರೆ, ಇದರ ಪರಿಣಾಮವಾಗಿ ಎಲೆಕ್ಟ್ರಾನ್ಗಳು ಬಿಡುಗಡೆಯಾಗುತ್ತವೆ. ಬ್ಯಾಟರಿಯನ್ನು ಚಾರ್ಜ್ ಮಾಡುವಾಗ, ಸಾಮಾನ್ಯ ಪರಿಸ್ಥಿತಿಗಳಲ್ಲಿ ಸಂಭವಿಸದ ವಸ್ತುಗಳ ಪರಸ್ಪರ ಕ್ರಿಯೆಯು ಸಂಭವಿಸುತ್ತದೆ. ರಾಸಾಯನಿಕ ಕ್ರಿಯೆಯ ಪರಿಣಾಮವಾಗಿ ವಸ್ತುವಿನಲ್ಲಿ ವಿದ್ಯುತ್ ಶೇಖರಣೆ ಎಂದು ಇದನ್ನು ಪರಿಗಣಿಸಬಹುದು. ವಿಸರ್ಜನೆಯ ಸಮಯದಲ್ಲಿ, ರಿವರ್ಸ್ ರೂಪಾಂತರವು ಪ್ರಾರಂಭವಾಗುತ್ತದೆ, ಇದು ವ್ಯವಸ್ಥೆಯನ್ನು ಆರಂಭಿಕ ಸ್ಥಿತಿಗೆ ಕಾರಣವಾಗುತ್ತದೆ. ಈ ಎರಡು ಪ್ರಕ್ರಿಯೆಗಳು ಒಟ್ಟಾಗಿ ಒಂದು ಚಾರ್ಜ್-ಡಿಸ್ಚಾರ್ಜ್ ಚಕ್ರವನ್ನು ರೂಪಿಸುತ್ತವೆ.
ನಿರ್ದಿಷ್ಟ ಉದಾಹರಣೆಯನ್ನು ಬಳಸಿಕೊಂಡು ಮೇಲಿನ ಪ್ರಕ್ರಿಯೆಯನ್ನು ನೋಡೋಣ - ಲೀಡ್-ಆಸಿಡ್ ಬ್ಯಾಟರಿ. ನೀವು ಊಹಿಸುವಂತೆ, ಈ ಪ್ರಸ್ತುತ ಮೂಲವು ಸೀಸವನ್ನು ಹೊಂದಿರುವ ಅಂಶವನ್ನು ಒಳಗೊಂಡಿರುತ್ತದೆ (ಹಾಗೆಯೇ ಸೀಸದ ಡೈಆಕ್ಸೈಡ್ PbO 2) ಮತ್ತು ಆಮ್ಲ. ಯಾವುದೇ ಬ್ಯಾಟರಿಯು ವಿದ್ಯುದ್ವಾರಗಳನ್ನು ಒಳಗೊಂಡಿರುತ್ತದೆ ಮತ್ತು ಅವುಗಳ ನಡುವಿನ ಅಂತರವು ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯದಿಂದ ತುಂಬಿರುತ್ತದೆ. ಎರಡನೆಯದಾಗಿ, ನಾವು ಈಗಾಗಲೇ ಕಂಡುಕೊಂಡಂತೆ, ನಮ್ಮ ಉದಾಹರಣೆಯಲ್ಲಿ ನಾವು ಸಲ್ಫ್ಯೂರಿಕ್ ಆಮ್ಲವನ್ನು 40 ಪ್ರತಿಶತದಷ್ಟು ಸಾಂದ್ರತೆಯೊಂದಿಗೆ ಬಳಸುತ್ತೇವೆ. ಅಂತಹ ಬ್ಯಾಟರಿಯ ಕ್ಯಾಥೋಡ್ ಸೀಸದ ಡೈಆಕ್ಸೈಡ್ನಿಂದ ಮಾಡಲ್ಪಟ್ಟಿದೆ, ಮತ್ತು ಆನೋಡ್ ಶುದ್ಧ ಸೀಸವನ್ನು ಹೊಂದಿರುತ್ತದೆ. ಇದೆಲ್ಲವೂ ಏಕೆಂದರೆ ಈ ಎರಡು ವಿದ್ಯುದ್ವಾರಗಳಲ್ಲಿ ಆಮ್ಲವು ವಿಭಜನೆಯಾದ ಅಯಾನುಗಳ ಭಾಗವಹಿಸುವಿಕೆಯೊಂದಿಗೆ ವಿಭಿನ್ನ ಹಿಮ್ಮುಖ ಪ್ರತಿಕ್ರಿಯೆಗಳು ನಡೆಯುತ್ತವೆ:
- PbO 2 + SO 4 2- + 4H + + 2e - = PbSO 4 + 2H 2 O (ಋಣಾತ್ಮಕ ವಿದ್ಯುದ್ವಾರದಲ್ಲಿ ಸಂಭವಿಸುವ ಪ್ರತಿಕ್ರಿಯೆ - ಕ್ಯಾಥೋಡ್).
- Pb + SO 4 2- - 2e - = PbSO 4 (ಧನಾತ್ಮಕ ವಿದ್ಯುದ್ವಾರದಲ್ಲಿ ಸಂಭವಿಸುವ ಪ್ರತಿಕ್ರಿಯೆ - ಆನೋಡ್).
ನಾವು ಪ್ರತಿಕ್ರಿಯೆಗಳನ್ನು ಎಡದಿಂದ ಬಲಕ್ಕೆ ಓದಿದರೆ, ಬ್ಯಾಟರಿಯನ್ನು ಡಿಸ್ಚಾರ್ಜ್ ಮಾಡಿದಾಗ ಸಂಭವಿಸುವ ಪ್ರಕ್ರಿಯೆಗಳನ್ನು ನಾವು ಪಡೆಯುತ್ತೇವೆ ಮತ್ತು ಬಲದಿಂದ ಎಡಕ್ಕೆ, ಬ್ಯಾಟರಿ ಚಾರ್ಜ್ ಮಾಡಿದಾಗ ಸಂಭವಿಸುವ ಪ್ರಕ್ರಿಯೆಗಳನ್ನು ನಾವು ಪಡೆಯುತ್ತೇವೆ. ಈ ಪ್ರತಿಯೊಂದು ಪ್ರತಿಕ್ರಿಯೆಗಳಲ್ಲಿ, ಈ ಪ್ರತಿಕ್ರಿಯೆಗಳು ವಿಭಿನ್ನವಾಗಿವೆ, ಆದರೆ ಅವುಗಳ ಸಂಭವಿಸುವಿಕೆಯ ಕಾರ್ಯವಿಧಾನವನ್ನು ಸಾಮಾನ್ಯವಾಗಿ ಒಂದೇ ರೀತಿಯಲ್ಲಿ ವಿವರಿಸಲಾಗಿದೆ: ಎರಡು ಪ್ರಕ್ರಿಯೆಗಳು ಸಂಭವಿಸುತ್ತವೆ, ಅವುಗಳಲ್ಲಿ ಒಂದರಲ್ಲಿ ಎಲೆಕ್ಟ್ರಾನ್ಗಳು "ಹೀರಿಕೊಳ್ಳುತ್ತವೆ", ಮತ್ತು ಇನ್ನೊಂದರಲ್ಲಿ, ಇದಕ್ಕೆ ವಿರುದ್ಧವಾಗಿ, " ಬಿಟ್ಟುಬಿಡು". ಅತ್ಯಂತ ಮುಖ್ಯವಾದ ವಿಷಯವೆಂದರೆ ಹೀರಿಕೊಳ್ಳುವ ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ಸಂಖ್ಯೆಯು ಬಿಡುಗಡೆಯಾದ ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ಸಂಖ್ಯೆಗೆ ಸಮಾನವಾಗಿರುತ್ತದೆ.
ವಾಸ್ತವವಾಗಿ, ಬ್ಯಾಟರಿಗಳ ಜೊತೆಗೆ, ಈ ವಸ್ತುಗಳಿಗೆ ಹಲವು ಅನ್ವಯಗಳಿವೆ. ಸಾಮಾನ್ಯವಾಗಿ, ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳು, ನಾವು ನೀಡಿದ ಉದಾಹರಣೆಗಳೆಂದರೆ, ಈ ಪದದ ಅಡಿಯಲ್ಲಿ ಒಂದಾಗಿರುವ ವಿವಿಧ ಪದಾರ್ಥಗಳ ಧಾನ್ಯ ಮಾತ್ರ. ಅವರು ಎಲ್ಲೆಡೆ, ಎಲ್ಲೆಡೆ ನಮ್ಮನ್ನು ಸುತ್ತುವರೆದಿರುತ್ತಾರೆ. ಇಲ್ಲಿ, ಉದಾಹರಣೆಗೆ, ಮಾನವ ದೇಹ. ಈ ವಸ್ತುಗಳು ಇಲ್ಲ ಎಂದು ನೀವು ಭಾವಿಸುತ್ತೀರಾ? ನೀವು ತುಂಬಾ ತಪ್ಪಾಗಿ ಭಾವಿಸಿದ್ದೀರಿ. ಅವು ನಮ್ಮಲ್ಲಿ ಎಲ್ಲೆಡೆ ಕಂಡುಬರುತ್ತವೆ, ಮತ್ತು ದೊಡ್ಡ ಪ್ರಮಾಣದ ರಕ್ತ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳಿಂದ ಮಾಡಲ್ಪಟ್ಟಿದೆ. ಉದಾಹರಣೆಗೆ, ಕಬ್ಬಿಣದ ಅಯಾನುಗಳು ಸೇರಿವೆ, ಇದು ಹಿಮೋಗ್ಲೋಬಿನ್ನ ಭಾಗವಾಗಿದೆ ಮತ್ತು ನಮ್ಮ ದೇಹದ ಅಂಗಾಂಶಗಳಿಗೆ ಆಮ್ಲಜನಕವನ್ನು ಸಾಗಿಸಲು ಸಹಾಯ ಮಾಡುತ್ತದೆ. ನೀರು-ಉಪ್ಪು ಸಮತೋಲನ ಮತ್ತು ಹೃದಯದ ಕಾರ್ಯವನ್ನು ನಿಯಂತ್ರಿಸುವಲ್ಲಿ ರಕ್ತದ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳು ಪ್ರಮುಖ ಪಾತ್ರವಹಿಸುತ್ತವೆ. ಈ ಕಾರ್ಯವನ್ನು ಪೊಟ್ಯಾಸಿಯಮ್ ಮತ್ತು ಸೋಡಿಯಂ ಅಯಾನುಗಳು ನಿರ್ವಹಿಸುತ್ತವೆ (ಪೊಟ್ಯಾಸಿಯಮ್-ಸೋಡಿಯಂ ಪಂಪ್ ಎಂಬ ಜೀವಕೋಶಗಳಲ್ಲಿ ಸಂಭವಿಸುವ ಪ್ರಕ್ರಿಯೆಯೂ ಇದೆ).
ನೀವು ಸ್ವಲ್ಪ ಕರಗಿಸಬಹುದಾದ ಯಾವುದೇ ವಸ್ತುಗಳು ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳಾಗಿವೆ. ಮತ್ತು ಅವರು ಬಳಸದ ಉದ್ಯಮ ಅಥವಾ ನಮ್ಮ ಜೀವನ ಯಾವುದೇ ಶಾಖೆ ಇಲ್ಲ. ಇದು ಕೇವಲ ಕಾರ್ ಬ್ಯಾಟರಿಗಳು ಮತ್ತು ಬ್ಯಾಟರಿಗಳು ಅಲ್ಲ. ಇವುಗಳು ಯಾವುದೇ ರಾಸಾಯನಿಕ ಮತ್ತು ಆಹಾರ ಉತ್ಪಾದನೆ, ಮಿಲಿಟರಿ ಕಾರ್ಖಾನೆಗಳು, ಬಟ್ಟೆ ಕಾರ್ಖಾನೆಗಳು, ಇತ್ಯಾದಿ.
ಮೂಲಕ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯದ ಸಂಯೋಜನೆಯು ಬದಲಾಗುತ್ತದೆ. ಹೀಗಾಗಿ, ಆಮ್ಲೀಯ ಮತ್ತು ಕ್ಷಾರೀಯ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳನ್ನು ಪ್ರತ್ಯೇಕಿಸಬಹುದು. ಅವುಗಳ ಗುಣಲಕ್ಷಣಗಳಲ್ಲಿ ಅವು ಮೂಲಭೂತವಾಗಿ ವಿಭಿನ್ನವಾಗಿವೆ: ನಾವು ಈಗಾಗಲೇ ಹೇಳಿದಂತೆ, ಆಮ್ಲಗಳು ಪ್ರೋಟಾನ್ ದಾನಿಗಳು ಮತ್ತು ಕ್ಷಾರಗಳು ಸ್ವೀಕರಿಸುವವರು. ಆದರೆ ಕಾಲಾನಂತರದಲ್ಲಿ, ವಸ್ತುವಿನ ಭಾಗದ ನಷ್ಟದಿಂದಾಗಿ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯದ ಸಂಯೋಜನೆಯು ಕಡಿಮೆಯಾಗುತ್ತದೆ ಅಥವಾ ಹೆಚ್ಚಾಗುತ್ತದೆ (ಇದು ಎಲ್ಲಾ ಕಳೆದುಹೋದ, ನೀರು ಅಥವಾ ಎಲೆಕ್ಟ್ರೋಲೈಟ್ ಅನ್ನು ಅವಲಂಬಿಸಿರುತ್ತದೆ).
ನಾವು ಪ್ರತಿದಿನ ಅವುಗಳನ್ನು ಎದುರಿಸುತ್ತೇವೆ, ಆದರೆ ಎಲೆಕ್ಟ್ರೋಲೈಟ್ಗಳಂತಹ ಪದದ ವ್ಯಾಖ್ಯಾನವನ್ನು ಕೆಲವರು ನಿಖರವಾಗಿ ತಿಳಿದಿದ್ದಾರೆ. ನಾವು ನಿರ್ದಿಷ್ಟ ವಸ್ತುಗಳ ಉದಾಹರಣೆಗಳನ್ನು ನೋಡಿದ್ದೇವೆ, ಆದ್ದರಿಂದ ಸ್ವಲ್ಪ ಹೆಚ್ಚು ಸಂಕೀರ್ಣ ಪರಿಕಲ್ಪನೆಗಳಿಗೆ ಹೋಗೋಣ.

ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳ ಭೌತಿಕ ಗುಣಲಕ್ಷಣಗಳು
ಈಗ ಭೌತಶಾಸ್ತ್ರದ ಬಗ್ಗೆ. ಈ ವಿಷಯವನ್ನು ಅಧ್ಯಯನ ಮಾಡುವಾಗ ಅರ್ಥಮಾಡಿಕೊಳ್ಳಬೇಕಾದ ಪ್ರಮುಖ ವಿಷಯವೆಂದರೆ ಎಲೆಕ್ಟ್ರೋಲೈಟ್ಗಳಲ್ಲಿ ಪ್ರಸ್ತುತವು ಹೇಗೆ ಹರಡುತ್ತದೆ. ಇದರಲ್ಲಿ ಅಯಾನುಗಳು ನಿರ್ಣಾಯಕ ಪಾತ್ರವನ್ನು ವಹಿಸುತ್ತವೆ. ಈ ಚಾರ್ಜ್ಡ್ ಕಣಗಳು ದ್ರಾವಣದ ಒಂದು ಭಾಗದಿಂದ ಇನ್ನೊಂದು ಭಾಗಕ್ಕೆ ಚಾರ್ಜ್ ಅನ್ನು ವರ್ಗಾಯಿಸಬಹುದು. ಹೀಗಾಗಿ, ಅಯಾನುಗಳು ಯಾವಾಗಲೂ ಧನಾತ್ಮಕ ವಿದ್ಯುದ್ವಾರಕ್ಕೆ ಒಲವು ತೋರುತ್ತವೆ, ಮತ್ತು ಕ್ಯಾಟಯಾನುಗಳು - ಋಣಾತ್ಮಕವಾಗಿರುತ್ತವೆ. ಹೀಗಾಗಿ, ವಿದ್ಯುತ್ ಪ್ರವಾಹದೊಂದಿಗೆ ಪರಿಹಾರದ ಮೇಲೆ ಕಾರ್ಯನಿರ್ವಹಿಸುವ ಮೂಲಕ, ನಾವು ಸಿಸ್ಟಮ್ನ ವಿವಿಧ ಬದಿಗಳಲ್ಲಿ ಶುಲ್ಕಗಳನ್ನು ಪ್ರತ್ಯೇಕಿಸುತ್ತೇವೆ.
ಬಹಳ ಆಸಕ್ತಿದಾಯಕ ಭೌತಿಕ ಲಕ್ಷಣವೆಂದರೆ ಸಾಂದ್ರತೆ. ನಾವು ಚರ್ಚಿಸುತ್ತಿರುವ ಸಂಯುಕ್ತಗಳ ಅನೇಕ ಗುಣಲಕ್ಷಣಗಳು ಇದನ್ನು ಅವಲಂಬಿಸಿರುತ್ತದೆ. ಮತ್ತು ಪ್ರಶ್ನೆಯು ಆಗಾಗ್ಗೆ ಉದ್ಭವಿಸುತ್ತದೆ: "ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯದ ಸಾಂದ್ರತೆಯನ್ನು ಹೇಗೆ ಹೆಚ್ಚಿಸುವುದು?" ವಾಸ್ತವವಾಗಿ, ಉತ್ತರ ಸರಳವಾಗಿದೆ: ದ್ರಾವಣದಲ್ಲಿ ನೀರಿನ ಅಂಶವನ್ನು ಕಡಿಮೆ ಮಾಡುವುದು ಅವಶ್ಯಕ. ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯದ ಸಾಂದ್ರತೆಯು ಹೆಚ್ಚಾಗಿ ನಿರ್ಧರಿಸಲ್ಪಟ್ಟಿರುವುದರಿಂದ, ಇದು ಹೆಚ್ಚಾಗಿ ನಂತರದ ಸಾಂದ್ರತೆಯ ಮೇಲೆ ಅವಲಂಬಿತವಾಗಿರುತ್ತದೆ. ನಿಮ್ಮ ಯೋಜನೆಯನ್ನು ಸಾಧಿಸಲು ಎರಡು ಮಾರ್ಗಗಳಿವೆ. ಮೊದಲನೆಯದು ತುಂಬಾ ಸರಳವಾಗಿದೆ: ಬ್ಯಾಟರಿಯಲ್ಲಿ ಒಳಗೊಂಡಿರುವ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯವನ್ನು ಕುದಿಸಿ. ಇದನ್ನು ಮಾಡಲು, ನೀವು ಅದನ್ನು ಚಾರ್ಜ್ ಮಾಡಬೇಕಾಗುತ್ತದೆ ಇದರಿಂದ ಒಳಗೆ ತಾಪಮಾನವು ಕೇವಲ ನೂರು ಡಿಗ್ರಿ ಸೆಲ್ಸಿಯಸ್ಗೆ ಏರುತ್ತದೆ. ಈ ವಿಧಾನವು ಸಹಾಯ ಮಾಡದಿದ್ದರೆ, ಚಿಂತಿಸಬೇಡಿ, ಇನ್ನೊಂದು ಇದೆ: ಹಳೆಯ ಎಲೆಕ್ಟ್ರೋಲೈಟ್ ಅನ್ನು ಹೊಸದರೊಂದಿಗೆ ಬದಲಾಯಿಸಿ. ಇದನ್ನು ಮಾಡಲು, ನೀವು ಹಳೆಯ ದ್ರಾವಣವನ್ನು ಹರಿಸಬೇಕು, ಬಟ್ಟಿ ಇಳಿಸಿದ ನೀರಿನಿಂದ ಉಳಿದಿರುವ ಸಲ್ಫ್ಯೂರಿಕ್ ಆಮ್ಲದಿಂದ ಒಳಭಾಗವನ್ನು ಸ್ವಚ್ಛಗೊಳಿಸಿ, ತದನಂತರ ಹೊಸ ಭಾಗವನ್ನು ತುಂಬಿಸಿ. ನಿಯಮದಂತೆ, ಉತ್ತಮ ಗುಣಮಟ್ಟದ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯ ಪರಿಹಾರಗಳು ತಕ್ಷಣವೇ ಬಯಸಿದ ಸಾಂದ್ರತೆಯನ್ನು ಹೊಂದಿರುತ್ತವೆ. ಬದಲಿ ನಂತರ, ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯದ ಸಾಂದ್ರತೆಯನ್ನು ಹೇಗೆ ಹೆಚ್ಚಿಸುವುದು ಎಂಬುದರ ಬಗ್ಗೆ ನೀವು ದೀರ್ಘಕಾಲದವರೆಗೆ ಮರೆತುಬಿಡಬಹುದು.
ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯದ ಸಂಯೋಜನೆಯು ಅದರ ಗುಣಲಕ್ಷಣಗಳನ್ನು ಹೆಚ್ಚಾಗಿ ನಿರ್ಧರಿಸುತ್ತದೆ. ವಿದ್ಯುತ್ ವಾಹಕತೆ ಮತ್ತು ಸಾಂದ್ರತೆಯಂತಹ ಗುಣಲಕ್ಷಣಗಳು, ಉದಾಹರಣೆಗೆ, ದ್ರಾವಕದ ಸ್ವರೂಪ ಮತ್ತು ಅದರ ಸಾಂದ್ರತೆಯ ಮೇಲೆ ಬಲವಾಗಿ ಅವಲಂಬಿತವಾಗಿರುತ್ತದೆ. ಬ್ಯಾಟರಿಯು ಎಷ್ಟು ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯವನ್ನು ಹೊಂದಿರುತ್ತದೆ ಎಂಬುದರ ಬಗ್ಗೆ ಪ್ರತ್ಯೇಕ ಪ್ರಶ್ನೆಯಿದೆ. ವಾಸ್ತವವಾಗಿ, ಅದರ ಪರಿಮಾಣವು ಉತ್ಪನ್ನದ ಘೋಷಿತ ಶಕ್ತಿಗೆ ನೇರವಾಗಿ ಸಂಬಂಧಿಸಿದೆ. ಬ್ಯಾಟರಿಯೊಳಗೆ ಹೆಚ್ಚು ಸಲ್ಫ್ಯೂರಿಕ್ ಆಮ್ಲ, ಅದು ಹೆಚ್ಚು ಶಕ್ತಿಯುತವಾಗಿರುತ್ತದೆ, ಅಂದರೆ, ಅದು ಹೆಚ್ಚು ವೋಲ್ಟೇಜ್ ಅನ್ನು ಉತ್ಪಾದಿಸುತ್ತದೆ.

ಇದು ಎಲ್ಲಿ ಉಪಯುಕ್ತವಾಗಿದೆ?
ನೀವು ಕಾರು ಉತ್ಸಾಹಿ ಅಥವಾ ಕಾರುಗಳಲ್ಲಿ ಆಸಕ್ತಿ ಹೊಂದಿದ್ದರೆ, ನೀವೇ ಎಲ್ಲವನ್ನೂ ಅರ್ಥಮಾಡಿಕೊಳ್ಳುತ್ತೀರಿ. ಈಗ ಬ್ಯಾಟರಿಯಲ್ಲಿ ಎಷ್ಟು ಎಲೆಕ್ಟ್ರೋಲೈಟ್ ಇದೆ ಎಂಬುದನ್ನು ನಿರ್ಧರಿಸುವುದು ಹೇಗೆ ಎಂದು ನಿಮಗೆ ತಿಳಿದಿದೆ. ಮತ್ತು ನೀವು ಕಾರುಗಳಿಂದ ದೂರವಿದ್ದರೆ, ಈ ವಸ್ತುಗಳ ಗುಣಲಕ್ಷಣಗಳು, ಅವುಗಳ ಬಳಕೆ ಮತ್ತು ಅವು ಪರಸ್ಪರ ಹೇಗೆ ಸಂವಹನ ನಡೆಸುತ್ತವೆ ಎಂಬುದರ ಜ್ಞಾನವು ಅತಿಯಾಗಿರುವುದಿಲ್ಲ. ಇದನ್ನು ತಿಳಿದುಕೊಂಡು ಬ್ಯಾಟರಿಯಲ್ಲಿ ಎಲೆಕ್ಟ್ರೋಲೈಟ್ ಏನಿದೆ ಎಂದು ಹೇಳಲು ಕೇಳಿದರೆ ನೀವು ಗೊಂದಲಕ್ಕೀಡಾಗುವುದಿಲ್ಲ. ಆದಾಗ್ಯೂ, ನೀವು ಕಾರು ಉತ್ಸಾಹಿಯಲ್ಲದಿದ್ದರೂ, ನೀವು ಕಾರನ್ನು ಹೊಂದಿದ್ದರೂ ಸಹ, ಬ್ಯಾಟರಿ ರಚನೆಯ ಜ್ಞಾನವು ಅತಿಯಾಗಿರುವುದಿಲ್ಲ ಮತ್ತು ರಿಪೇರಿ ಮಾಡಲು ನಿಮಗೆ ಸಹಾಯ ಮಾಡುತ್ತದೆ. ಆಟೋ ಸೆಂಟರ್ಗೆ ಹೋಗುವುದಕ್ಕಿಂತ ಎಲ್ಲವನ್ನೂ ನೀವೇ ಮಾಡಲು ಇದು ತುಂಬಾ ಸುಲಭ ಮತ್ತು ಅಗ್ಗವಾಗಿದೆ.
ಮತ್ತು ಈ ವಿಷಯವನ್ನು ಉತ್ತಮವಾಗಿ ಅಧ್ಯಯನ ಮಾಡಲು, ಶಾಲೆ ಮತ್ತು ವಿಶ್ವವಿದ್ಯಾಲಯಗಳಿಗೆ ರಸಾಯನಶಾಸ್ತ್ರ ಪಠ್ಯಪುಸ್ತಕವನ್ನು ಓದಲು ನಾವು ಶಿಫಾರಸು ಮಾಡುತ್ತೇವೆ. ನೀವು ಈ ವಿಜ್ಞಾನವನ್ನು ಚೆನ್ನಾಗಿ ತಿಳಿದಿದ್ದರೆ ಮತ್ತು ಸಾಕಷ್ಟು ಪಠ್ಯಪುಸ್ತಕಗಳನ್ನು ಓದಿದ್ದರೆ, ವರಿಪೇವ್ ಅವರ "ರಾಸಾಯನಿಕ ಪ್ರಸ್ತುತ ಮೂಲಗಳು" ಉತ್ತಮ ಆಯ್ಕೆಯಾಗಿದೆ. ಬ್ಯಾಟರಿಗಳು, ವಿವಿಧ ಬ್ಯಾಟರಿಗಳು ಮತ್ತು ಹೈಡ್ರೋಜನ್ ಕೋಶಗಳ ಕಾರ್ಯಾಚರಣೆಯ ಸಂಪೂರ್ಣ ಸಿದ್ಧಾಂತವನ್ನು ಅಲ್ಲಿ ವಿವರವಾಗಿ ವಿವರಿಸಲಾಗಿದೆ.
ತೀರ್ಮಾನ
ನಾವು ಕೊನೆಯ ಹಂತಕ್ಕೆ ಬಂದಿದ್ದೇವೆ. ಸಾರಾಂಶ ಮಾಡೋಣ. ಎಲೆಕ್ಟ್ರೋಲೈಟ್ಗಳಂತಹ ಪರಿಕಲ್ಪನೆಗೆ ಸಂಬಂಧಿಸಿದ ಎಲ್ಲವನ್ನೂ ನಾವು ಮೇಲೆ ಚರ್ಚಿಸಿದ್ದೇವೆ: ಉದಾಹರಣೆಗಳು, ರಚನೆ ಮತ್ತು ಗುಣಲಕ್ಷಣಗಳ ಸಿದ್ಧಾಂತ, ಕಾರ್ಯಗಳು ಮತ್ತು ಅಪ್ಲಿಕೇಶನ್ಗಳು. ಮತ್ತೊಮ್ಮೆ, ಈ ಸಂಯುಕ್ತಗಳು ನಮ್ಮ ಜೀವನದ ಭಾಗವಾಗಿದೆ ಎಂದು ಹೇಳುವುದು ಯೋಗ್ಯವಾಗಿದೆ, ಅದು ಇಲ್ಲದೆ ನಮ್ಮ ದೇಹಗಳು ಮತ್ತು ಉದ್ಯಮದ ಎಲ್ಲಾ ಕ್ಷೇತ್ರಗಳು ಅಸ್ತಿತ್ವದಲ್ಲಿಲ್ಲ. ರಕ್ತದ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳ ಬಗ್ಗೆ ನಿಮಗೆ ನೆನಪಿದೆಯೇ? ಅವರಿಗೆ ಧನ್ಯವಾದಗಳು ನಾವು ಬದುಕುತ್ತೇವೆ. ನಮ್ಮ ಕಾರುಗಳ ಬಗ್ಗೆ ಏನು? ಈ ಜ್ಞಾನದಿಂದ, ಬ್ಯಾಟರಿಗೆ ಸಂಬಂಧಿಸಿದ ಯಾವುದೇ ಸಮಸ್ಯೆಯನ್ನು ನಾವು ಸರಿಪಡಿಸಬಹುದು, ಏಕೆಂದರೆ ಅದರಲ್ಲಿ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯದ ಸಾಂದ್ರತೆಯನ್ನು ಹೇಗೆ ಹೆಚ್ಚಿಸುವುದು ಎಂದು ನಾವು ಈಗ ಅರ್ಥಮಾಡಿಕೊಂಡಿದ್ದೇವೆ.
ಎಲ್ಲವನ್ನೂ ಹೇಳುವುದು ಅಸಾಧ್ಯ, ಮತ್ತು ನಾವು ಅಂತಹ ಗುರಿಯನ್ನು ಹೊಂದಿಸಲಿಲ್ಲ. ಎಲ್ಲಾ ನಂತರ, ಈ ಅದ್ಭುತ ವಸ್ತುಗಳ ಬಗ್ಗೆ ಹೇಳಲಾಗುವುದಿಲ್ಲ.
- ಏಳು ವರ್ಷಗಳ ಯುದ್ಧದಲ್ಲಿ ರಷ್ಯಾದ ಪಡೆಗಳು
- ಬ್ಯಾಲೆನ್ಸ್ ಶೀಟ್: ಲೆಕ್ಕಪತ್ರ ನಿರ್ವಹಣೆಯಲ್ಲಿ ಇದರ ಅರ್ಥ ಖಾತೆ 20 ಗಾಗಿ ಪ್ರಾಥಮಿಕ ದಾಖಲೆಗಳು
- ಸಾಂಸ್ಥಿಕ ಆಸ್ತಿ ತೆರಿಗೆ: ಮುಂಗಡ ಪಾವತಿಯ ಗಡುವು ಯಾವಾಗ ಆಸ್ತಿ ತೆರಿಗೆಯನ್ನು ಪಾವತಿಸಲಾಗುತ್ತದೆ?
- ಪ್ಲಾಟನ್ ವ್ಯವಸ್ಥೆ: BU ಮತ್ತು NU ನಲ್ಲಿ ಆಯೋಜಕರು ಬಜೆಟ್ಗೆ ವರ್ಗಾಯಿಸಿದ “ಪ್ಲೇಟನ್” ಶುಲ್ಕದ ಲೆಕ್ಕಪತ್ರ ಪ್ರತಿಬಿಂಬ
- 1C ಲೆಕ್ಕಪತ್ರದಲ್ಲಿ ಒಂದು-ಬಾರಿ ಬೋನಸ್ ಅನ್ನು ಹೇಗೆ ಪಾವತಿಸುವುದು
- ಕುಟಾಫಿನಾದಲ್ಲಿ ಉತ್ತೀರ್ಣ ಸ್ಕೋರ್
- ಪ್ರವೇಶ ದಿನ ವರ್ಷದಲ್ಲಿ ವಿಶ್ವವಿದ್ಯಾನಿಲಯಗಳಲ್ಲಿ ದಾಖಲಾತಿ ದಿನಾಂಕಗಳು
- ಮೊದಲನೆಯದು ಚಂದ್ರ ಮತ್ತು ಮಂಗಳಕ್ಕೆ ಹಾರಲು ತುಸುರ್ ಮಾರ್ಗವಾಗಿದೆ
- ಆರ್ಗನೋಲೆಮೆಂಟ್ ಸಂಯುಕ್ತಗಳ ರಸಾಯನಶಾಸ್ತ್ರ ಆರ್ಗನೋಲೆಮೆಂಟ್ ಸಂಯುಕ್ತಗಳ ರಸಾಯನಶಾಸ್ತ್ರದ ಸಾಮಾನ್ಯ ಸಮಸ್ಯೆಗಳು
- ಲೆನಿನ್ನಿಂದ ಗೋರ್ಬಚೇವ್ಗೆ: ಎನ್ಸೈಕ್ಲೋಪೀಡಿಯಾ ಆಫ್ ಬಯೋಗ್ರಫಿಸ್
- ಚೆರ್ನಿಗೋವ್ ರೆಜಿಮೆಂಟ್ 1825 ರ ದಂಗೆ
- ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳು ಸೇರಿವೆ
- ಕತ್ತಿನ ತ್ರಿಕೋನಗಳು ಮತ್ತು ಅವುಗಳ ಪ್ರಾಯೋಗಿಕ ಮಹತ್ವ
- ಕೇಂದ್ರಾಪಗಾಮಿ: ವಿಧಾನದ ವಿಧಗಳು ಮತ್ತು ಅಪ್ಲಿಕೇಶನ್ ಕೇಂದ್ರಾಪಗಾಮಿ ವಿಧಾನವು ಆಧರಿಸಿದೆ
- UHF ಚಿಕಿತ್ಸೆ: ಸೂಚನೆಗಳು ಮತ್ತು ವಿರೋಧಾಭಾಸಗಳು, ಮಕ್ಕಳು, ವಯಸ್ಕರು
- ಶ್ರೋಣಿಯ ಮೂಳೆ: ಮಾನವ ಅಂಗರಚನಾಶಾಸ್ತ್ರ
- ನೈಸರ್ಗಿಕ ಪರಿಸ್ಥಿತಿಗಳು ಮತ್ತು ರಷ್ಯಾದ ಅಭಿವೃದ್ಧಿಯ ಮೇಲೆ ಅವುಗಳ ಪ್ರಭಾವ
- ಭೂಮಿ - ಸೌರವ್ಯೂಹದ ಗ್ರಹ
- ಟ್ವೆರ್ನಲ್ಲಿ ಮಂಗೋಲ್-ಟಾಟರ್ಗಳ ವಿರುದ್ಧ ದಂಗೆ (1327
- ಅಂತರ್ಯುದ್ಧ ಮತ್ತು ವಿದೇಶಿ ಹಸ್ತಕ್ಷೇಪ